
【题目】下列关于原电池的说法中,正确的是( )
A.任何化学反应上都能设计成原电池
B.原电池工作时,阳离子向负极移动
C.原电池的负极发生氧化反应
D.原电池工作时,电子通过电解质溶液流向正极
科目:高中化学 来源: 题型:
【题目】A、B、C、D为四种可溶性盐,它们的阳离子分别是此![]() 、
、![]() 、
、![]() 、
、![]() 中的一种,阴离子分别是
中的一种,阴离子分别是![]() 、
、![]() 、
、![]() 、
、![]() 中的一种(离子在物质中不能重复出现)。现做如下实验:
中的一种(离子在物质中不能重复出现)。现做如下实验:
①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈蓝色;
②向①的四支试管中分别加入盐酸, B的溶液中有沉淀生成, D的溶液中有无色无味的气体逸出。
根据①②实验现象回答下列问题:
(1)写出A、C的化学式:A__________,B__________,C_________。
(2)写出盐酸与D反应的离子方程式:_____________________________________。
(3)写出C与![]() 溶液反应的离子方程式:________________________________。
溶液反应的离子方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是中药黄芩中的主要活性成分之一,具有氧化和抗肿痛作用。G的合成路线如下图所示:
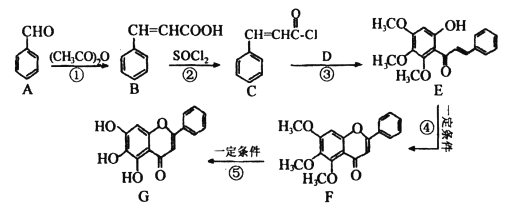
回答下列问题:
(1)写出G中含氧官能团的名称________;G的分子式为________。
(2)反应③的反应类型是______反应。
(3)D的分子式为C9H12O4,写出D的结构简式_________;同时符合下列条件的D的同分异构体有多种,请写出其中两种的结构简式_________。
a.属于苯的衍生物。苯环上共有4个取代基
b.核磁共振氢谱中有5种等效氢
c.与FeCl3溶液发生显色反应
(4)写出反应①化学方程式为___________。
(5)合成路线流程图示例: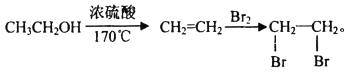 ,参照题中所给信息,任选试剂,由CH3CHO为原料合成
,参照题中所给信息,任选试剂,由CH3CHO为原料合成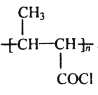 。______________________
。______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2018·安徽省合肥市高三第三次教学质量检测)H2S在重金属离子处理、煤化工等领域都有重要应用。请回答:
Ⅰ.H2S是煤化工原料气脱硫过程的重要中间体,反应原理为
ⅰ.COS(g)+H2(g)![]() H2S(g)+CO(g)△H=+7kJ·mol1
H2S(g)+CO(g)△H=+7kJ·mol1
ⅱ.CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=42kJ·mol1
CO2(g)+H2(g)△H=42kJ·mol1
已知断裂1mol气态分子中的化学键所需能量如下表所示。
分子 | COS(g) | H2(g) | CO(g) | H2S(g) |
能量(kJ·mol1) | 1310 | 442 | x | 669 |
(1)计算表中x=_______。
(2)T℃时,向VL容积不变的密闭容器中充入1mol COS(g)、1mol H2(g)和1mol H2O(g),发生上述两个反应。
①在T℃时测得平衡体系中COS为0.80 mol,H2为0.85 mol,则T℃时反应ⅰ的平衡常数K=_______(保留2位有效数字)。
②上述反应达平衡后,若向其中再充入1mol COS(g)、1molH2(g)和1mol H2O(g),则再次达平衡后H2的体积分数_______(填“增大”、“减小”或“不变”);若升高温度,则CO的平衡体积分数_______(填“增大”、“减小”或“不变”),其理由是_______。
Ⅱ.H2S在高温下分解制取H2,同时生成硫蒸气。
(3)向2L密闭容器中加入0.2molH2S,反应在不同温度(900~1500℃)下达到平衡时,混合气体中各组分的体积分数如下图所示,则在此温度区间内,H2S分解反应的主要化学方程式为_______;在1300℃时,反应经2min达到平衡,则0~2min的反应速率v(H2S)=_______。
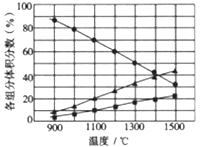
Ⅲ.H2S用作重金属离子的沉淀剂。
(4)25℃时,向浓度均为0.001mol·L1Sn2+和Ag+的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Ag+)=_______。(已知:25℃时,Ksp(SnS)=1.0×1025,Ksp(Ag2S)=1.6×1049)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.有机物A的结构简式是 ,它可以通过不同的反应得到下列物质:
,它可以通过不同的反应得到下列物质:
B. 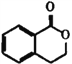 C.
C. 
D.  E.
E. 
(1)A中含氧官能团的名称:_____________________________。
(2)写出由A制取B的化学方程式:_____________________________。
(3)写出A制取C、D、二种物质的有机反应类型:
A制C:_____________反应,A 制 D :_________________反应
(4)写出一种既可以看做酯类又可以看做酚类,且分子中苯环上连有三种取代基的A的同分异构体的结构简式:______________________________。
Ⅱ.F、G都是有机化合物,请回答下列问题:
(1)已知:6.0g化合物F完全燃绕生成8.8gCO2和3.6gH2O;F的蒸气对氢气的相对密度为30,则F的分子式为__________________________。
(2)G的分子式是C8H8Br2,在G的同分异构体中,苯环上一硝化的产物只有一种的共有_______个,其中核磁共振氢谱有两组峰,且峰面职比为l∶l的是_______(填结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】诺卜醇可用于调制木香型化妆品及皂用香精。一种制备方法如图所示,下列说法正确的是
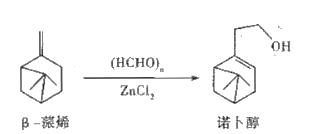
A. 可用溴的CCl4溶液区别β-蒎烯与诺卜醇
B. β-蒎烯的饱和碳原子上的一氯代物最多有7种
C. β-蒎烯和诺卜醇分子中都有一个由5个碳原子构成的四面体
D. 可用乙酸检验β-蒎烯是否含有诺卜醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2X的溶液中只有一种分子,但存在HX-、X2-等四种离子。常温下向20mL0.2mol/L的H2X溶液中滴加0.2mol/L的NaOH溶液,滴加过程中溶液pH与滴入的NaOH溶液体积关系如图所示,下列说法中正确的是
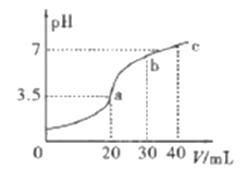
A. X2-+H2O![]() HX-+OH-的平衡常数Kb≈1×10-8
HX-+OH-的平衡常数Kb≈1×10-8
B. a点的溶液中:c(X2-)+c(HX-)<0.1mol/L
C. c点时溶液中:c(Na+)>c(X2-)>c(HX-)>c(OH-)>c(H+)
D. b点时n(Na+)>n(X2-)=n(HX-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A的相对分子质量为84,分子中含有碳碳双键,且分子中只有一种类型的氢。
(1)A的结构简式为____________________。
(2)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。

C的化学名称是_______________;E2的结构简式是_______________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com