
下列说法中,正确的是
| A.离子化合物中,阴、阳离子间存在静电吸引力 |
| B.HF、HCl、HBr和HI的热稳定性和还原性从左到右依次减弱 |
| C.第三周期非金属元素对应的含氧酸从左到右依次增强 |
| D.短周期元素形成离子后,最外层电子数都达到8电子稳定结构 |
科目:高中化学 来源: 题型:单选题
甲、乙、丙、丁为四种主族元素,甲元素与乙、丙、丁三种元素相邻,甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20。下列判断正确的是
| A.原子半径:丙>乙>甲>丁 |
| B.气态氢化物的稳定性:甲>丙 |
| C.最高价氧化物对应的水化物的酸性:丁>甲 |
| D.乙和甲或乙和丁所能形成的化合物都是剧毒物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X是第三周期非金属元素,该原子如果要达到8电子稳定结构,需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是
| A.X最高价氧化物对应的水化物不一定是强酸 |
| B.X元素的氢化物化学式一定为H2X |
| C.X的单质—定是良好的半导体材料 |
| D.X元素的氧化物—定能与烧碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知A、B、C、D为短周期主族元素,其相对位置关系如图。C与B可形成离子化合 物C3B2。下列分析正确的是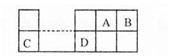
A.电负性:C>A
B.离子氧化性:C>D
C.氢化物稳定性:A> B
D.原子半径:r(C)> r(B)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如下图。下列说法正确的是
| A.五种元素中,原子半径最大的是W |
| B.Y与Z形成的化合物都可以和盐酸反应 |
| C.Y的简单阴离子比W的简单阴离子还原性强 |
| D.Z与Q形成的化合物水溶液一定显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
据科学家预测,月球的土壤中吸附着数百万吨的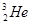 ,而在地球上氦元素则主要以
,而在地球上氦元素则主要以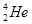 的形式存在。下列说法正确的是
的形式存在。下列说法正确的是
A.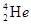 原子核内含有4个质子 原子核内含有4个质子 |
B.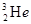 与 与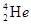 互为同位素 互为同位素 |
C.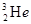 与 与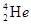 在元素周期表中占有不同的位置 在元素周期表中占有不同的位置 |
D.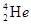 的最外层电子数为2,故 的最外层电子数为2,故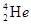 易失去最外层电子 易失去最外层电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
利用中学所学相关规律,下列推断正确的一项是
| A.碳酸钡的溶解度略大于硫酸钡,向硫酸钡的饱和溶液中加入较多的碳酸钠固体,会有碳酸钡生成 |
B.某温度T时,水的离子积常数为KW,该温度下将V1mLa mol?L-1的一元酸HA与V2mLb mol?L-1的一元碱BOH充分混合,若混合溶液中c(OH-)= mol?L-1,则此溶液不一定呈中性 mol?L-1,则此溶液不一定呈中性 |
| C.ⅣA族元素形成的氢化物的沸点从上到下依次递增,则ⅤA族元素所形成的氢化物的沸点从上到下也是依次递增 |
D.依据反应2C+SiO2 2CO↑+Si ,还原性:Si <C 2CO↑+Si ,还原性:Si <C |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
图中是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R﹤W |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH >Ba(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com