
 根据下式所示的氧化还原反应设计一个原电池:Fe+2Fe3+═3Fe2+
根据下式所示的氧化还原反应设计一个原电池:Fe+2Fe3+═3Fe2+分析 由方程式可知,反应中只有Fe元素化合价变化,则负极应为Fe,发生氧化反应生成Fe2+,正极为活泼性比铁弱的金属或非金属,发生还原反应,Fe3+被还原生成Fe2+,则电解质为FeCl3,以此解答该题.
解答 解:(1)由方程式可知,反应中只有Fe元素化合价变化,则负极应为Fe,发生氧化反应生成Fe2+,正极为活泼性比铁弱的金属或非金属,发生还原反应,Fe3+被还原生成Fe2+,则电解质为FeCl3,则此原电池的装置图为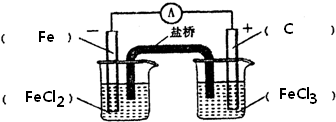 ,
,
故答案为: ;
;
(2)负极为Fe,发生氧化反应生成Fe2+,电极反应式为Fe-2e-=Fe2+,正极为活泼性比铁弱的金属或非金属,可为碳棒,发生还原反应,Fe3+被还原生成Fe2+,电极方程式为2Fe3++2e-=2Fe2+,
答:负极:Fe-2e-=Fe2+;正极:2Fe3++2e-=2Fe2+.
点评 本题考查原电池的设计及原电池的工作原理,题目难度不大,注意从氧化还原反应的角度由电池反应判断电极反应.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案科目:高中化学 来源: 题型:解答题


 ;
; +CH3CH(OH)CH2CH2OH$→_{△}^{浓硫酸}$
+CH3CH(OH)CH2CH2OH$→_{△}^{浓硫酸}$ +2H2O;
+2H2O; .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.25mol/L | B. | 7mol/L | C. | 7.5mol/L | D. | 12.5mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com