
同温同压下,下列各组热化学方程式中,ΔH1<ΔH2的是( )
A.S(g)+O2(g)=SO2(g) ΔH1S(s)+O2(g)=SO2(g) ΔH2
B.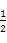 H2(g)+
H2(g)+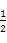 Cl2(g)=HCl(g) ΔH1H2(g)+Cl2(g)=2HCl(g) ΔH2
Cl2(g)=HCl(g) ΔH1H2(g)+Cl2(g)=2HCl(g) ΔH2
C.2H2(g)+O2(g)=2H2O(g) ΔH12H2(g)+O2(g)=2H2O(l) ΔH2
D.C(s)+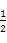 O2(g)=CO(g) ΔH1C(s)+O2(g)=CO2(g) ΔH2
O2(g)=CO(g) ΔH1C(s)+O2(g)=CO2(g) ΔH2
科目:高中化学 来源:2014高考化学二轮专题突破 专题一物质的组成性质和分类练习卷(解析版) 题型:选择题
下图是某反应在密闭容器中反应前后的分子状况示意图,“●”和“○”分别表示不同的原子。下列对该过程的相关描述正确的是( )
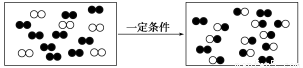
A.有一种物质过量 B.发生的是分解反应
C.发生的是置换反应 D.生成了两种产物
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题7电解质溶液练习卷(解析版) 题型:选择题
下列说法正确的是( )
A.常温下醋酸分子不可能存在于pH>7的碱性溶液中
B.常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中c(N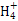 )>c(Cl-)
)>c(Cl-)
C.0.1 mol·L-1的氯化铵溶液与0.05 mol·L-1的氢氧化钠溶液等体积混合后溶液中离子浓度的大小关系是:c(Cl-)>c(N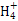 )>c(Na+)>c(OH-)>c(H+)
)>c(Na+)>c(OH-)>c(H+)
D.0.1 mol·L-1硫化钠溶液中离子浓度的关系:c(Na+)=c(S2-)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题5物质结构 元素周期律练习卷(解析版) 题型:选择题
已知X、Y、Z、W、R五种元素,原子序数依次增大,且原子序数都小于20,X元素的原子是所有元素的原子中半径最小的,Y、W同主族,Z、W同周期,Y元素原子的最外层电子数是次外层的3倍,Z、R分别是同周期中金属性最强的元素。下列说法不正确的是( )
A.沸点:X2Y>X2W
B.由X、Y、Z、W四种元素组成的化合物既含有共价键又含离子键
C.原子半径:X<Y<Z<W<R
D.Y与W形成的化合物WY2是形成酸雨的主要物质之一
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题4化学反应中的能量变化练习卷(解析版) 题型:填空题
Ⅰ.利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。用乙烯作为还原剂将氮的氧化物还原为N2是燃煤烟气的一种脱硝(除NOx)技术。其脱硝机理如图所示。写出该脱硝过程中乙烯和NO2反应的化学方程式 。
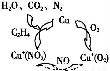
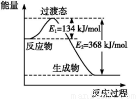
Ⅱ.(1)如图是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是 (填“增大”、“减小”或“不变”,下同),ΔH的变化是 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1;
②CH3OH(g)+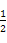 O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1。
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1。
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1。
则甲醇蒸气完全燃烧生成液态水的热化学方程式为 。
写出甲醇质子交换膜燃料电池在酸性条件下的负极反应式: 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题3氧化还原反应 离子反应练习卷(解析版) 题型:填空题
Ⅰ.磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子结构示意图是 。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2 6CaSiO3+P4O10
6CaSiO3+P4O10
10C+P4O10 P4+10CO
P4+10CO
每生成1 mol P4时,就有 mol电子发生转移。
(3)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2 C6H6O6+2H++2I-
C6H6O6+2H++2I-
2S2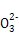 +I2
+I2 S4
S4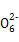 +2I-
+2I-
在一定体积的某维生素C溶液中加入a mol/L I2溶液V1 mL,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗b mol/L Na2S2O3溶液V2 mL。该溶液中维生素C的物质的量是 mol。
(4)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:
2I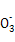 +5S
+5S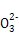 +2H+
+2H+ I2+5S
I2+5S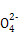 +H2O
+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。
某同学设计实验如下表所示:
| 0.01 mol/LKIO3酸性溶液(含淀粉)的体积/mL | 0.01 mol/LNa2SO3溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液出现蓝色时所需时间/s |
实验1 | 5 | V1 | 35 | 25 |
|
实验2 | 5 | 5 | 40 | 25 |
|
实验3 | 5 | 5 | V2 | 0 |
|
该实验的目的是 ;表中V2= mL。
Ⅱ.稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(5)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中,NH4Cl的作用是 。
(6)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
Ce3++ H2O2+ H2O Ce(OH)4↓+ 。
Ce(OH)4↓+ 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题3氧化还原反应 离子反应练习卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是( )
A.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O Al
Al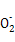 +4N
+4N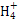 +2H2O
+2H2O
B.用FeCl3溶液腐蚀铜线电路板:Cu+2Fe3+ Cu2++2Fe2+
Cu2++2Fe2+
C.大理石溶于醋酸中的反应:CaCO3+2H+ Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
D.钠与水反应:Na+2H2O Na++2OH-+H2↑
Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题1物质的组成性质分类和化学用语练习卷(解析版) 题型:填空题
以下是依据一定的分类标准,对某些物质与水反应情况进行分类的图示。
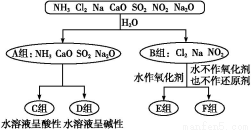
请根据你所学的知识,按要求填空:
(1)上述第一级分类标准(分成A、B组的依据)是 。
(2)F组中物质除了Cl2外还有 (填化学式)。
(3)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类型为 (用序号填空)。
①金属氧化物;②碱性氧化物;③碱;④碱性干燥剂
CaO可作干燥剂的理由是 (用化学方程式表示)。
(4)D组中NH3的水溶液呈弱碱性,用电离方程式表示其呈弱碱性的原因: 。
(5)由Al3+制备Al(OH)3,最好不选择D组中的NaOH溶液,说明理由: 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题11常见有机物及其应用练习卷(解析版) 题型:选择题
下列与有机物的结构、性质有关的叙述正确的是( )
A.苯、油脂均不能使酸性KMnO4溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.葡萄糖、果糖的分子式均为C6H12O6,两者互为同分异构体
D.乙醇、乙酸均能与Na反应放出H2,两者分子中官能团相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com