
 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1 2CO2(g);ΔH 2
2CO2(g);ΔH 2 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3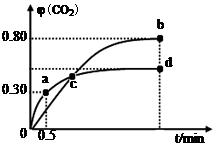
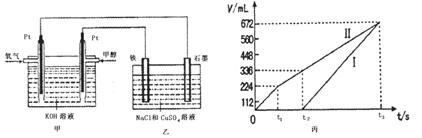
| A.容器内气体密度不变,表明反应达到平衡状态 |
| B.两种温度下,c点时体系中混合气体的平均相对分子质量相等 |
| C.增加I2O5的投料量有利于提高CO的转化率 |
| D.b点和d点的化学平衡常数:Kb<Kd |
 5CO2(g)+I2(s)
5CO2(g)+I2(s) 

科目:高中化学 来源:不详 题型:填空题
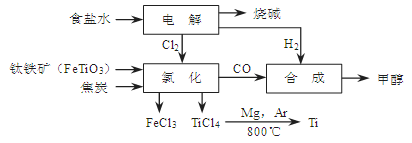
 CH3OH(g)。
CH3OH(g)。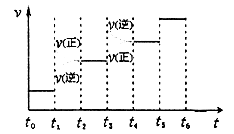
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe3O4 | B.Fe2O3 | C.Fe5O7 | D.Fe4O5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8:11 | B.3:5 | C.1:2 | D.9:4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.S2O32-是还原剂 |
| B.Y的化学式为Fe2O3 |
| C.a=4 |
| D.每有1 mol O2参加反应,转移的电子总数为4 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1mol | B.0.03mol | C.0.02mol | D.0.04mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④ | B.②③ | C.①③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.12 | B.5.34 | C.7.26 | D.8.23 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 )与季戊四醇(
)与季戊四醇( )以物质的量之比2:1反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X的核磁共振氢蛮如下图所示:
)以物质的量之比2:1反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X的核磁共振氢蛮如下图所示:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com