
分析 (1)根据化合价代数和为0计算;
(2)Fe3C在足量的空气中高温煅烧生成四氧化三铁和二氧化碳;磁性固体能溶于过量盐酸发生反应生成氯化铁、氯化亚铁和水;
(3)由离子反应关系,银离子物质的量等于氯离子物质的量,据此计算0.54g FeClx中氯离子物质的量计算x值;根据Ksp(Ag2CrO4)=1.12×10-12计算c(CrO42-).
解答 解:(1)因为K2FeO4中化合价代数和为0,其中K为+1,O为-2,所以铁元索的化合价为+6,故答案为:+6;
(2)Fe3C在足量的空气中高温煅烧生成四氧化三铁和二氧化碳,反应为Fe3C+3O2$\frac{\underline{\;高温\;}}{\;}$Fe3O4+CO2;磁性固体能溶于过量盐酸发生反应生成氯化铁、氯化亚铁和水,离子反应为Fe3O4+8H+=2Fe3++Fe2++4H2O,
故答案为:Fe3C+3O2$\frac{\underline{\;高温\;}}{\;}$Fe3O4+CO2;Fe3O4+8H+=2Fe3++Fe2++4H2O;
(3)n(Cl-)=n(Ag+)=0.01994L×0.5 mol•L-1=0.01 mol,则$\frac{0.54g}{(56+35.5x)g/mol}$•x=0.010 mol,解得x=3;又Ksp(Ag2CrO4)=1.12×10-12,c(Ag+)=2.0×10-5mol•L-1,则c(CrO42-)=$\frac{1.12×10{\;}^{-12}}{(2.0×10{\;}^{-5}){\;}^{2}}$=0.0028mol•L-1,
故答案为:3;0.0028.
点评 本题考查滴定计算、混合物计算、方程式的书写等,难度中等,侧重分析能力与计算能力的综合考查.


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | Na2SO4[H2SO4] | B. | KBr[H2O] | C. | 盐酸[HCl] | D. | Cu(NO3)2[Cu(OH)2] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 日常生活中常用75%的乙醇溶液来杀菌消毒 | |
| B. | 可用淀粉溶液来检测食盐中是否含碘 | |
| C. | 发酵粉中主要含有碳酸钠,能使焙制出的糕点疏松多孔 | |
| D. | 医院中常用碳酸钡作为内脏造影剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,10g46%的CH3CH2OH溶液中所含有的氧原子数为0.4NA | |
| B. | 向FeI2溶液中通人适量的Cl2,当有1molFe2+被氧化时,共转移电子数目为3NA | |
| C. | 在标准状况下,将11.2LHCl溶于1L水中,溶液中HCl分子数为0.5NA | |
| D. | 常温常压下,0.1molNaHSO4晶体中,含有阴阳离子数共0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色中性溶液中:Na+、K+、CO32-、SO42- | |
| B. | 含有大量Fe3+的溶液中:Na+、Mg2+、NO3-、I- | |
| C. | 加入铝粉后有气体放出的溶液:Fe2+、K+、NO3-、Cl- | |
| D. | 能使酚酞变红色的溶液:CO32-、Cl-、F-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

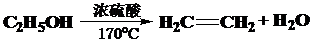 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com