

| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应II 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
分析 Ⅰ、依据热化学方程式和盖斯定律计算所得热化学方程式;
Ⅱ、(1)①自发进行的判断依据是△H-T△S<0,结合反应特征分析判断需要的条件;
②平衡标志是正逆反应速率相同,个组分含量保持不变,原则是变量不变分析选项;
③图象t2起点,t3 到t4终点,t4以后符合变化趋势即可,在t2时将容器容积缩小一倍,压强增大,二氧化碳浓度增大,平衡正向进行,随后减小,t3时达到平衡,t4时降低温度,平衡正向进行,二氧化碳减小,反应速率减小,t5时达到平衡;
(2)①CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,反应Ⅰ是恒温恒容容器,Ⅱ为恒容绝热,反应是放热反应,图表中反应ⅠⅡ若恒温恒容达到相同平衡状态,Ⅱ为逆向恒容绝热,温度降低,平衡正向进行,平衡常数增大,甲醇浓度增大;
②反应速率V=$\frac{△c}{△t}$计算得到氢气反应速率,速率之比等于化学方程式计量数之比计算甲醇反应速率;依据平衡三段式列式计算分析平衡状态的物质的量.
解答 解:Ⅰ. 已知:H2的热值为142.9KJ•g-1 ,燃烧热为285.8KJ/mol,
①H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8KJ/mol
②N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
③H2O(g)=H2O(l)△H=-44kJ•mol-1
①×4-②-③×4得到催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1;
故答案为:4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1;
Ⅱ.(1)①CO2(g)+3H2(g)═CH3OH(l)+H2O(l),熵变△S<0,则反应焓变△H<0,低温下满足△H-T△S<0
故答案为:低温;
②CO2(g)+3H2(g)═CH3OH(l)+H2O(l),
a、混合气体的平均式量始终保持不变,不能说明反应达到平衡状态,故a错误;
b、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,所以过程中CO2和H2的体积分数始终保持不变,故b错误;
c、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,CO2和H2的转化率始终相等,不能确定反应是否达到平衡状态,故c错误;
d、反应物是气体,生成物是液体,混合气体的密度保持不变,说明反应达到平衡状态,故d正确;
e、1mol CO2生成的同时有3mol H-H键断裂,说明正逆反应速率相同,反应达到平衡状态,故e正确;
故答案为:de;
③在t2时将容器容积缩小一倍,压强增大,二氧化碳浓度增大,平衡正向进行,随后减小,t3时达到平衡,t4时降低温度,平衡正向进行,二氧化碳减小,反应速率减小,t5时达到平衡;
图象t2起点二氧化碳浓度突然增大为1mol/L,随反应进行减小,图中t3 到t4终点平衡线在0.5的线上,t4t4以后在0.5线以下,但不能到横坐标线上且有平衡线段,图象为: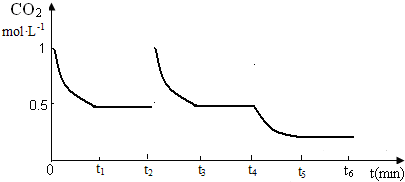 ;
;
故答案为:
(2)①CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,反应Ⅰ是恒温恒容容器,Ⅱ为恒容绝热,反应是放热反应,图表中反应ⅠⅡ若恒温恒容达到相同平衡状态,Ⅱ为逆向恒容绝热,温度降低,平衡正向进行,平衡常数增大,甲醇浓度增大;
故答案为:<,<;
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)
起始量(mol) 2 6 0 0
变化量(mol) 1 3 1 1
30min量(mol) 1 3 1 1
对反应I,前10min内的平均反应速率v(CH3OH)=$\frac{1}{3}$V(H2)=$\frac{1}{3}$×(6-4.5)mol2L10min=0.025mol•L-1•min-1;
若30min时只改变温度为T2℃,此时H2的物质的量为3.2mol,氢气增加,说明平衡逆向进行,温度升高T2>T1,
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)
起始量(mol/L)1 3 0 0
变化量(mol/L)0.5 1.5 0.5 0.5
30min量(mol/L)0.5 1.5 0.5 0.5
浓度商Q1=$\frac{0.5×0.5}{0.5×1.{5}^{3}}$=$\frac{0.5}{1.{5}^{3}}$
若30min时只向容器中再充入1mol CO2(g)和1mol H2O(g),
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)
(mol/L)1 1.5 0.5 1
浓度商Q2=$\frac{1×0.5}{1×1.{5}^{3}}$=$\frac{0.5}{1.{5}^{3}}$=Q1,
所以平衡不移动;
故答案为:0.025mol•L-1•min-1 ,<,不.
点评 本题考查了热化学方程式书写,平衡影响因素分析判断,平衡计算的分析应用,注意恒温恒容和恒容绝热容器的分析判断,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y |
| A | SO2 | NH3 |
| B | Cl2 | CO2 |
| C | NH3 | CO2 |
| D | SO2 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,则H2的标准燃烧热为-241.8 kJ•mol-1 | |
| B. | 若C(石墨,s)=C(金刚石,s)△H>0,则石墨比金刚石稳定 | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ•mol-1,则20.0g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量 | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用澄清石灰水来区分二氧化碳和二氧化硫 | |
| B. | 用米汤检验食用加碘盐(含KIO3)中含有碘元素 | |
| C. | 能使灼热的CuO由黑变红的气体一定是H2 | |
| D. | 可用石蕊试液来鉴别盐酸和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨和氯化钠分别受热熔化 | B. | 冰的融化和水的分解 | ||
| C. | NaCl和HCl溶于水 | D. | 干冰和碘的升华 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(NO3)2+H2SO4═BaSO4↓+2HNO3 | B. | BaCl2+Na2SO4═BaSO4↓+2NaCl | ||
| C. | Ba(OH)2+K2SO4═BaSO4↓+2KOH | D. | Ba(OH)2+H2SO4═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:Na+、MnO4-、CO32-、Cl- | |
| B. | 能使紫色石蕊试剂变红的溶液中:OH-、K+、Ba2+、Na+ | |
| C. | 透明的酸性溶液中:Fe3+、Mg2+、Cl-、NO3- | |
| D. | pH=1的溶液中:NH4+、Fe2+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com