
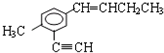
 中,同一平面上碳原子最多数目和同一直线上的碳原子最多数目分别为( )
中,同一平面上碳原子最多数目和同一直线上的碳原子最多数目分别为( )| A. | 11、4 | B. | 10、3 | C. | 12、4 | D. | 13、4 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行共线、共面分析判断,注意单键可以旋转.
解答 解:在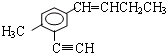 分子中,甲基中C原子处于苯中H原子的位置;苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙基中连接双键的C原子处于碳碳双键形成的平面,乙基中的亚甲基具有四面体结构,乙基中甲基C原子通过旋转碳碳单键可能处于碳碳双键形成的平面,乙炔基为直线结构,处于苯环的平面结构;故苯环中6个C原子、甲基中1个C原子、乙炔基中2个C原子、碳碳双键中2个C原子、乙基中2个C原子,可能处于同一平面,所以最多有13个C原子;有机物
分子中,甲基中C原子处于苯中H原子的位置;苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙基中连接双键的C原子处于碳碳双键形成的平面,乙基中的亚甲基具有四面体结构,乙基中甲基C原子通过旋转碳碳单键可能处于碳碳双键形成的平面,乙炔基为直线结构,处于苯环的平面结构;故苯环中6个C原子、甲基中1个C原子、乙炔基中2个C原子、碳碳双键中2个C原子、乙基中2个C原子,可能处于同一平面,所以最多有13个C原子;有机物 中,处于共线的碳原子最多的是:乙炔基、乙炔基连接的苯环C原子及该C原子对称的苯环C原子,故最多有4个C原子共线,故选D.
中,处于共线的碳原子最多的是:乙炔基、乙炔基连接的苯环C原子及该C原子对称的苯环C原子,故最多有4个C原子共线,故选D.
点评 本题考查有机物结构中共面、共线问题,难度中等,关键是空间想象,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,单键可以旋转.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
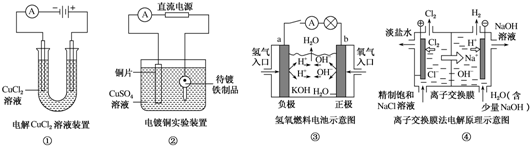
| A. | ①装置中阴极处产生的气体能够使湿润KI淀粉试纸变蓝 | |
| B. | ②装置中待镀铁制品应与电源正极相连 | |
| C. | ③装置中电子由b极流向a极 | |
| D. | ④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
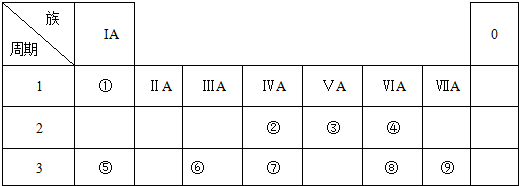
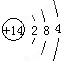 .
.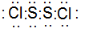 ;A可与水反应生成刺激性气味且能使品红溶液褪色的气体及其他生成物,写出该反应化学方程式:2S2Cl2+2H2O=SO2↑+3S↓+4HCl.
;A可与水反应生成刺激性气味且能使品红溶液褪色的气体及其他生成物,写出该反应化学方程式:2S2Cl2+2H2O=SO2↑+3S↓+4HCl.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
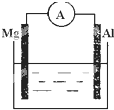 根据所学知识回答下列问题,在如图所示装置中
根据所学知识回答下列问题,在如图所示装置中查看答案和解析>>
科目:高中化学 来源: 题型:解答题
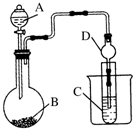 某化学兴趣小组利用如图装置验证元素非金属性的变化规律.
某化学兴趣小组利用如图装置验证元素非金属性的变化规律.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
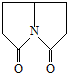
| A. | 一氯取代物有5种 | B. | 二氯取代物有8种 | C. | 可发生水解反应 | D. | 该物质中有羰基 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com