
分析 (1)该有机物对空气的相对密度为2,则有机物相对分子质量=29×2=58;
(2)5.8g有机物的物质的量为0.1mol,燃烧生成CO2和H2O气且体积比为1:1,碱石灰在增加18.6g为CO2和H2O的质量,计算二者物质的量,根据原子守恒计算分子中C、H原子数目,再根据相对分子质量计算O原子数目,进而确定有机物分子式.
解答 解:(1)空气的平均分子量为29,相对密度与相对分子质量成正比,该有机物对空气的相对密度为2,则有机物相对分子质量为:29×2=58,
答:该有机物的相对分子质量为58;
(2)5.8g有机物的物质的量为:$\frac{5.8g}{58g/mol}$=0.1mol,完全燃烧生成CO2和H2O气且体积比为1:1,碱石灰在增加18.6g为CO2和H2O的质量,则18n(H2O)+44n(CO2)=18.6,解得:n(CO2)=n(H2O)=$\frac{18.6}{44n+18n}$mol=0.3mol,
则有机物分子中N(C)=$\frac{0.3mol}{0.1mol}$═3、N(H)=$\frac{0.3mol×2}{0.1mol}$=6、N(O)=$\frac{58-12×3-6}{16}$=1,
故有机物分子式为:C3H6O,
答:该有机物分子式为C3H6O.
点评 本题考查了有机物分子式的确定,题目难度中等,明确相对密度与相对分子质量的关系为解答关键,注意掌握质量守恒在确定有机物分子式中的应用方法.


科目:高中化学 来源: 题型:选择题
| A. | Rn的原子核内中子数与质子数的差值为50 | |
| B. | Rn位于元素周期表中第六周期0族 | |
| C. | Rn的最外层电子排布式为6s26p6,化学性质不活泼 | |
| D. | 新铺大理石地面的居室,不用打开门窗换气,因为氡对人体无危害 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
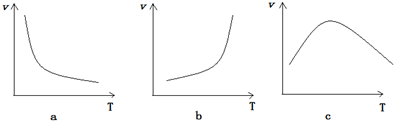
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 甲 | 乙 | 丙 | |
| 所含元素 | C、H | C、H、F | C、H、F |
| 所含电子数 | 26 | ||
| 结构特点 | 饱和有机物 | ||
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加压 | B. | 加催化剂 | C. | 降温 | D. | 升温 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L O3含有分子的数目为NA | |
| B. | 常温常压下,4.0 g CH4中含有共价键的数目为NA | |
| C. | 在密闭容器中加入1.5 mol H2和0.5 molN2,充分反应后可得到NH3分子数为NA | |
| D. | 标准状况下,2.24 L Cl2与足量NaOH溶液反应,转移电子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮分子是双原子分子 | B. | 氮元素的非金属性很强 | ||
| C. | 氮原子的半径较小 | D. | 氮分子中的化学键很难破坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴、阳离子间通过静电引力而形成的化学键称为离子键 | |
| B. | 在MgO和CO2 晶体中都不存在单个分子 | |
| C. | 金属中存在自由移动的带电微粒,所以能导电 | |
| D. | 离子晶体中存在带电微粒,所以能导电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com