
某同学用Na2CO3配制0.1mol/L的Na2CO3溶液的过程如图所示,其中错误的操作有

⑤ ⑥ ⑦
A. ①⑤⑥ B. ②④⑦ C. ①⑥ D. ⑤⑥⑦
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源:2015-2016学年山东省高一上10月月考化学卷(解析版) 题型:选择题
相同状况下,20mL气体A2和10mL气体B2恰好化合生成20mL气体C,则C的化学式为
A.AB B.AB2
C.A2B D.A4B2
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次月考化学试卷(解析版) 题型:选择题
化学与生活、社会发展息息相关,下列有关说法不正确的是
A.食盐可作调味剂,也可作食品防腐剂
B.Na2O2和Na2O均可常用作呼吸面具中的供氧剂
C.“熬胆矾铁釜,久之亦化为铜”,是因为熬制过程发生了置换反应
D.古剑“沈卢”“以剂钢为刃”柔铁为蒸干,不尔则多断折”,剂钢是指铁合金
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次考试化学试卷(解析版) 题型:选择题
下列各组中的两种物质相互反应时,无论哪种过量,都可用同一个离子方程式表示的是( )
① 碳酸钠溶液与盐酸 ② 硫化氢气体与氯化铁溶液
③ 硫酸铝溶液与氨水 ④ 碳酸氢钙溶液与澄清石灰水
⑤ 碘化亚铁溶液与氯水
A.②③ B.①③④ C.②④ D.②③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上第一次月考化学卷(解析版) 题型:填空题
(1)质量之比为16∶7∶6的三种气体SO2、CO、NO,分子个数之比为________;氧原子个数之比为________;相同条件下体积比为________。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92g该氧化物的体积为448ml,则该氧化物的摩尔质量为________,R的相对原子质量为________。RO2的化学式为_____________
(3)常温下,在27.5g水中溶解12.5gCuSO4·5H2O,恰好达到饱和,该溶液的密度为1.21 g/cm3,则该溶液中CuSO4的物质的量浓度_________________,从中取出20.0 mL该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是_____________ml。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上第一次月考化学卷(解析版) 题型:选择题
下列溶液中的Cl-浓度与50ml1mol·L-1 MgCl2溶液中的Cl-浓度相等的是
A.75mL2mol•L-1 CaCl2溶液
B.150mL2mol•L-1NaCl溶液
C.150mL2mol•L-1KClO3溶液
D.75mL1mol•L-1 AlCl3溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上第一次月考化学卷(解析版) 题型:选择题
现有三组实验:①含有水分的植物油中除去水分:②回收碘CC14溶液中CC14 ;③用食用酒精浸泡中草药提取其中的有效成分。分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
下列关于热化学反应的描述中正确的是
A.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0kJ/mol
B.1mol甲烷燃烧生成水蒸汽和二氧化碳所放出的热量是甲烷燃烧热
C.已知由石墨制备金刚石为吸热反应,则金刚石比石墨稳定
D.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上10月月考化学卷(解析版) 题型:填空题
Ⅰ.金刚石和石墨均为碳的同素异形体,它们燃烧时,若氧气不足生成一氧化碳,若充分燃烧生成二氧化碳,反应中放出的热量如图所示。
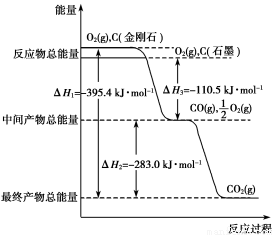
(1)等质量的金刚石和石墨完全燃烧,____________(填“金刚石”或“石墨”)放出的热量更多,写出表示石墨燃烧热的热化学方程式:_______________________。注意:石墨用“C(石墨,s)”表示。
(2)在通常状况下,____________(填“金刚石”或“石墨”)更稳定。
(3)6 g石墨在一定量空气中燃烧,生成气体18 g,该过程中放出的热量为______________kJ。
Ⅱ.白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
(1)已知298 K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2 983.2 kJ·mol-1
4P(红磷,s)+5O2(g)= 4 P4O10(s) ΔH2=-2954 kJ·mol-1
则该温度下白磷转化为红磷的热化学方程式:4P(红磷,s) ==P4(白磷,s)ΔH=____________
(2)已知298 K时白磷不完全燃烧的热化学方程式为:P4(白磷,s)+3O2(g)=P4O6(s) ΔH=-1 638 kJ·mol-1。在某密闭容器中加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为_________________,反应过程中放出的热量为___________kJ。
(3)已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):
P—P:198,Cl—Cl :243,P—Cl:331。
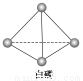
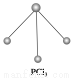
则反应P4(白磷,s)+6Cl2(g)=4PCl3(s)的反应热ΔH=_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com