
| A. | 明矾与漂白粉常用于自来水的净化与消毒,这两者的作用原理是一样的 | |
| B. | 为了防止中秋月饼的富脂食物因被氧化而变质,常在包装袋里放生石灰 | |
| C. | 海轮外壳上镶入锌块,可减缓船体的腐蚀,该方法叫牺牲阳极的阴极保护法 | |
| D. | 酸雨就是pH<7的雨水,主要是由大气中的SO2、NO2等造成的 |
分析 A.明矾中含有Al3+,水解呈酸性,生成Al(OH)3;漂白粉能与二氧化碳和水反应生成次氯酸,次氯酸具有强氧化性,可用于消毒;
B.为了防止中秋月饼的富脂食物因被氧化而变质,应加入还原性物质;
C.海轮外壳连接锌块,形成原电池,锌为负极;
D.酸雨PH值小于5.6.
解答 解:A.明矾中含有Al3+,水解呈酸性,生成Al(OH)3,Al(OH)3能吸附水中悬浮的杂质;氯漂白粉能与二氧化碳和水反应生成次氯酸,次氯酸具有强氧化性,可用于消毒,两者净化消毒两者原理不同,故A错误;
B.生石灰为氧化钙,不具有还原性,不能防止中秋月饼的富脂食物因被氧化而变质,故B错误;
C.海轮外壳连接锌块,锌为负极,保护外壳不受腐蚀,为牺牲阳极的阴极保护法,故C正确;
D.酸雨PH值小于5.6,故D错误.
故选:C.
点评 本题考查了金属的腐蚀与防护、明矾净水与漂白粉消毒的原理,明确原电池和电解池原理、明矾、次氯酸钙的性质是解本题关键,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
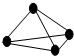 原子间以共价单键相连的非金属单质中,一个原子与相邻原子的成键数为8-N,N为该非金属元素的族序数,化学家把这一现象称为8-N规则.某非金属单质的结构如图所示,则构成该单质的元素位于( )
原子间以共价单键相连的非金属单质中,一个原子与相邻原子的成键数为8-N,N为该非金属元素的族序数,化学家把这一现象称为8-N规则.某非金属单质的结构如图所示,则构成该单质的元素位于( )| A. | ⅢA | B. | ⅣA | C. | ⅤA | D. | ⅥA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强酸和强碱的中和反应的活化能接近于零,所以反应速率很高 | |
| B. | 过程的自发性既能用于判断过程的方向,也能用于判断过程发生的速率 | |
| C. | 电解质溶液导电的过程中,一定发生了电解质溶液的电解 | |
| D. | 溶解度较小的BaSO4在一定条件下也可以转化为溶解度略大的BaCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 碱性: Mg (OH)2> Cu(OH)2 | 第一电离能:O< N | 熔点: MgS< MgO | 稳定性: H2S< H2O |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-c=m-n | B. | b+d=m+n | C. | a>b>d>c | D. | a>b>c>d |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com