
分析 具有相同质子数,不同中子数的不同原子互为同位素;
由同种元素形成的不同种单质互为同素异形体;
具有相同分子式而结构不同的化合物互为同分异构体.
解答 解:①金刚石与“足球烯”C60都是由碳元素形成的不同的单质,互为同素异形体;
②H2O与D2O组成和结构都相同,为同一物质;
③16O、17O、和18O 质子数相同,中子数不同,互为同位素;
④氧气(O2)与臭氧(O3)都是由O元素形成的不同单质,互为同素异形体;
⑤乙醇(CH3CH2OH)和甲醚(CH3OCH3)的分子式为C2H6O,结构不同,互为同分异构体;
故答案为:(1)①④;(2)③;(3)⑤.
点评 本题主要考查了同系物、同分异构体、同位素、同素异形体的区别,题目难度不大,注意把握概念的内涵与外延.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na2O2与CO2完全反应时转移电子数为2NA | |
| B. | 标准状况下11.2 L Cl2与4.25 g NH3所含有的原子数 | |
| C. | 标准状况下36 g H2O与1.204×1024个O2分子所占的体积 | |
| D. | 1mol固体NaHCO3所含有的阴阳离子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
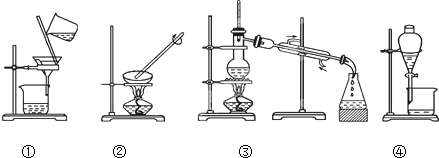
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如表所示:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如表所示:| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数(Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①②④ | C. | ②④⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
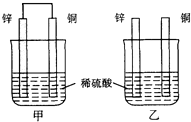
| A. | 两烧杯中铜片表面均有气泡产生 | B. | 甲中铜片是正极,锌片是负极 | ||
| C. | 两烧杯中溶液的pH均增大 | D. | 产生气泡的速度甲比乙快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量钠保存在汽油中 | |
| B. | 固态碘盛放在细口玻璃瓶中 | |
| C. | 液溴保存在加有少量水的盖有玻璃塞的棕色细口瓶中 | |
| D. | 浓硝酸盛放在盖有橡胶塞的棕色瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
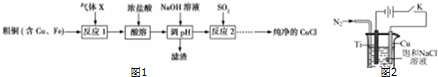
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com