
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A.c(H+)/c(OH-)=1×10-12的溶液中:![]()
B.0.1mol/LHCl溶液:![]()
C.0.1mol/LK2CO3溶液:![]()
D.c(Fe2+)=0.1mol/L溶液中:![]()
科目:高中化学 来源: 题型:
【题目】下列溶液中有关微粒的物质的量浓度关系正确的是( )
A.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(OH-)>c(H+)
B.常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7:c(Na+)>(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)=c(OH-)
C.常温下,pH=6的NaHSO3溶液中:c(SO32-)﹣c(H2SO3)=9.9×10-7molL-1
D.物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=2c(HCO3-)+2c(H2CO3)+2c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温、恒容下,有下列气体反应分别从两条途径进行:
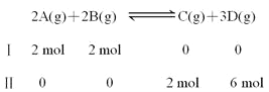
下列叙述正确的是( )
A. Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的百分组成相同
B. Ⅰ、Ⅱ两条途径最终达到平衡时,体系内混合气体的浓度相同
C. 达到平衡时,Ⅰ途径所用的时间与Ⅱ途径所用的时间相同
D. 达到平衡时,Ⅰ途径混合气体密度等于Ⅱ途径混合气体的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物G是合成维生素类药物的中间体,其结构简式如图1所示,G的合成路线如图2所示:
其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知:-CHO+
请回答下列问题:
(1)G的分子式是__,G中官能团的名称是__;
(2)第①步反应的化学方程式是__;
(3)B的名称(系统命名)是__;
(4)第②~⑥步反应中属于取代反应的有__(填步骤编号);
(5)第④步反应的化学方程式是________;
(6)写出同时满足下列条件的E的所有同分异构体的结构简式__,①只含一种官能团;②链状结构且无﹣O﹣O﹣;③核磁共振氢谱只有2种峰。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国首创以铝—空气—海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则:
(1)电源的负极材料是________,负极反应为___________;正极反应为___________。
(2)熔盐电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO32--4e-=4CO2,正极反应式为____________,电池总反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:
(1)2A(g) ![]() 2B(g)+C(g); (2)A(g)
2B(g)+C(g); (2)A(g) ![]() C(g)+D(g)。
C(g)+D(g)。
当达到平衡时,测得c(A)=2.5 mol·L-1(表示该物质浓度,下同),c(C)=2.0 mol·L-1。则下列说法中正确的是( )
A.达到平衡时A的总转化率为40%B.达到平衡时c(B)为1.0 mol·L-1
C.达到平衡时c(B)=2c(D)D.达到平衡时c(D)=2c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知图甲表示某温度下pH=l的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,图乙表示水在不同温度下的电离平衡曲线。下列有关图像的判断叙述正确的是
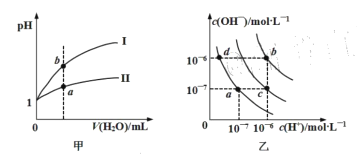
A.图甲中曲线II为盐酸
B.图甲中a点溶液的导电性比b点弱
C.图乙中纯水仅升高温度,就可以从a点变到c点
D.图乙中在b点对应温度下,将pH=2的H2SO4溶液与pH=10的NaOH溶液等体积混合后,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiCoO2用途广泛,如可作为锂离子电池的电极。回答下列问题。
(1)在周期表中,与Li的化学性质最相似的邻族元素是_________,该元素基态原子核外M层电子的自旋状态_________(填“相同”或“相反”)。
(2)[Co(NH3)6]Cl3是橙黄色晶体,该配合物中提供空轨道接受孤对电子的微粒是___,配体分子的价层电子对互斥模型为___,写出一种与配体分子互为等电子体的分子_________(填分子式)。
(3)某钴化合物纳米粉可以提高碱性电池的性能。该化合物晶胞结构如图所示,则该钴化合物的化学式为______,与Co原子等距离且最近的O原子个数为______。

(4)Li还可形成多种物质。二异丙基胺基锂(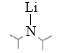 )是有机合成中常用的物质,氮原子的杂化方式为_________。Li+可以镶嵌在C60中,形成的[LiC60]PF6与NaCl具有类似的晶胞结构,下面是从某晶体结构中分割出来的部分结构图,其中属于从[LiC60]PF6晶体中分割出来的结构图是___。
)是有机合成中常用的物质,氮原子的杂化方式为_________。Li+可以镶嵌在C60中,形成的[LiC60]PF6与NaCl具有类似的晶胞结构,下面是从某晶体结构中分割出来的部分结构图,其中属于从[LiC60]PF6晶体中分割出来的结构图是___。
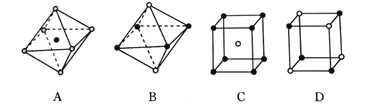
(5)金属锂晶体的结构为体心立方密堆积,晶胞边长为351 pm,则锂晶体中原子的空间利用率为_________(列出含π的计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铬绿(Cr2O3)的性质独特,在冶金、颜料等领域有着不可替代的地位。一种利用淀粉水热还原铬酸钠制备氧化铬绿的工艺流程如下:
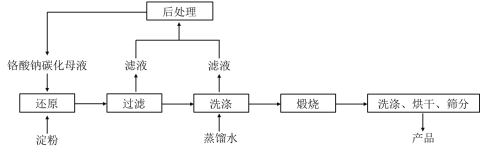
已知:①向含少量Na2CO3的铬酸钠碱性溶液中通入CO2可制得不同碳化率的铬酸钠碳化母液;
②“还原”反应剧烈放热,可制得Cr(OH)3浆料。
(1)该工艺中“还原”反应最初使用的是蔗糖或甲醛,后来改用价格低廉的淀粉。请写出甲醛(HCHO)与铬酸钠(Na2CrO4)溶液反应的离子方程式_________。
(2)将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列有关说法错误的是_____(填标号)。
A 该反应一定无需加热即可进行 B 必要时可使用冷却水进行温度控制
C 铬酸钠可适当过量,使淀粉充分反应 D 应建造废水回收池,回收含铬废水
(3)测得反应完成后在不同恒温温度、不同碳化率下Cr(Ⅵ)还原率如下图。实际生产过程中Cr(Ⅵ)还原率可高达99.5%以上,“还原”阶段采用的最佳反应条件为_________。
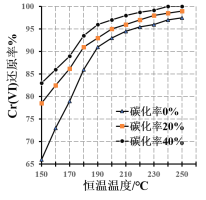
(4)滤液中所含溶质为_______。该水热法制备氧化铬绿工艺的优点有_________、________(请写出两条)。
(5)由水热法制备的氢氧化铬为无定型氢氧化铬[Cr(OH)3·nH2O]。将洗涤并干燥后的氢氧化铬滤饼充分煅烧,质量损失与固体残留质量比为9:19,经计算得出n=_________。
(6)重铬酸钠(Na2Cr2O7·H2O)与硫酸铵热分解法也是一种生产氧化铬绿的方法,生产过程中产生的气体对环境无害,其化学反应方程式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com