
实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表:
| 化合物 | 相对分子质量 | 密度/g·cm-3 | 沸点,/℃ | 溶解度/l00g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
操作如下:
①在50mL三颈烧瓶中,加入18.5 mL正丁醇和13.4 mL冰醋酸, 3~4滴浓硫酸,投入沸石。安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管。
②将分水器分出的酯层和反应液一起倒入分液漏斗中,水洗,10% Na2CO3洗涤,再水洗,最后转移至锥形瓶,干燥。
③将干燥后的乙酸正丁酯滤入烧瓶中,常压蒸馏,收集馏分,得15.1 g乙酸正丁酯。
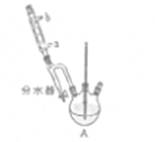
请回答有关问题:
(1)冷水应该从冷凝管 (填a或b)端管口通入。
(2)仪器A中发生反应的化学方程式为____ 。
(3)步骤①“不断分离除去反应生成的水”该操作的目的是: 。
(4)步骤②中,10%Na2CO3溶液洗涤有机层,该步操作的目的是 。
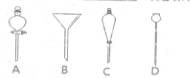
(5)进行分液操作时,使用的漏斗是 (填选项)。
(6)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏 (填“高”或者“低”)原因是____
(7)该实验过程中,生成乙酸正丁酯的产率是 。
【知识点】有机物的制备、混合物分离、除杂J1 J2 L6
【答案解析】(1)a(1分)
(2)CH3COOH+CH3CH2CH2CH2OH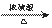 CH3COOCH2CH2CH2CH3+H2O(2分)
CH3COOCH2CH2CH2CH3+H2O(2分)
(3)使用分水器分离出水,使平衡正向移动,提高反应产率(2分);
(4)除去产品中含有的乙酸等杂质(2分)
(5)C(1分)
(6)高(1分) 会收集到少量未反应的冰醋酸和正丁醇(2分)
(7)65%(或65.1%) (2分)
解析:(1)为了保证冷凝效果冷水需要低进高出,所以应该从冷凝管a端管口通入。
(2)根据酯化反应的原理,羧基去羟基,醇去氢生成酯和水,仪器A中发生反应的化学方程式为:CH3COOH+CH3CH2CH2CH2OH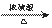 CH3COOCH2CH2CH2CH3+H2O。
CH3COOCH2CH2CH2CH3+H2O。
(3)利用减小生成物的浓度平衡正向移动,步骤①“不断分离除去反应生成的水”该操作的目的是使用分水器分离出水,使平衡正向移动,提高反应产率。
(4)步骤②中用10%Na2CO3溶液洗涤有机层,目的是除去产品中含有的乙酸等杂质。
(5)AC都是分液漏斗,A主要组装制气体的装置,进行分液操作时,使用的漏斗是C。
(6)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,由于会收集到少量未反应的冰醋酸和正丁醇似的产率偏高。
(7)18.5 mL正丁醇的质量是18.5 mL×0.8g/mL=14.8g,13.4 mL冰醋酸的质量是13.4 mL×1.045g/mL=14g,设理论上得到乙酸正丁酯的质量是x,
CH3COOH+CH3CH2CH2CH2OH CH3COOCH2CH2CH2CH3+H2O。
CH3COOCH2CH2CH2CH3+H2O。
60g 74g 116g
14g 14.8g x
CH3COOH过量,所以x=116g×14.8g÷74g=23.2g
生成乙酸正丁酯的产率是:15.1g÷23.2g×100%=65.1%
【思路点拨】本题考查了有机物的制备、分离、除杂,产率计算,难度不大。


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
某有机物的分子式为C8H8,经研究表明该有机物不能发生加成反应和加聚反应,在常温下难被酸性KMnO4溶液氧化,但在一定条件下却可与Cl2发生取代反应,而且其一氯代物只有一种。下列对该有机物结构的推断中一定正确的是( )
A.该有机物中含有碳碳双键
B.该有机物属于芳香烃
C.该有机物分子具有平面环状结构
D.该有机物具有三维空间的立体结构
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,萘可以被硝酸和硫酸的混合酸硝化生成二硝基物,它是1,5二硝基萘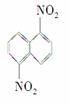 ,1,8二硝基萘
,1,8二硝基萘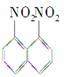 的混合物,后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可将这两种异构体分离。将上述硝化产物加入适量98%的硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8二硝基萘,应采用的方法是( )
的混合物,后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可将这两种异构体分离。将上述硝化产物加入适量98%的硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8二硝基萘,应采用的方法是( )
A.蒸发浓缩结晶
B.向滤液中加水过滤
C.用碳酸钠溶液处理滤液
D.将滤液缓缓加入水中
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
(1)该物质的结构简式为
________________________________________________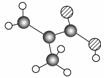 ________________________。
________________________。
(2)该物质中所含官能团的名称为________________________。
(3)下列物质中,与该产品互为同系物的是(填序号)________,互为同分异构体的是__________。
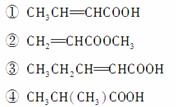
查看答案和解析>>
科目:高中化学 来源: 题型:
)有一瓶无色溶液,其中可能含有NH4+、K+ 、Mg2+、Ba2+、Al3+ 、Fe3+、I-、Cl-、NO3-、CO32-、SO42-取该溶液进行以下实验:
①该溶液可使pH试纸呈红色;
②取少量溶液加新制氯水及CCl4振荡,可见CCl4层呈现紫色;
③取少量溶液加氯化钡溶液,有白色沉淀生成,加人HNO3后沉淀不溶解;
④取实验③之上层清液,加入硝酸银溶液有白色沉淀生成,加入HNO3后沉淀不溶解;
⑤取少量原溶液加入NaOH溶液呈碱性,在此过程中有白色沉淀生成,而后又逐渐消失,将此溶液加热,有无色气休放出,该气体能使润湿的红色石蕊试纸变蓝。
根据上述实验事实,溶液中肯定存在的离子有_____________________,肯定不存在的离子有_____________________,不能确定是否存在的离子有_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
适用相关化学知识进行判断,下列结论正确的是
A.某吸热反应能自发进行,则该反应的△S>0
B.SO2使酸性KMnO4溶液褪色,因此SO2具有漂白性
C.在物质分离的方法中,蒸馏、萃取、重结晶都与物质的溶解度有关
D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能加快生成H2的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,错误的是( )
A.苯酚具有弱酸性,但不能使紫色石蕊变红
B.能因发生化学反应而使溴水褪色的物质一定是和溴水发生加成反应
C.用核磁共振氢谱鉴别1溴丙烷和2溴丙烷
D.含醛基的有机物都能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上由铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按下图所示流程进行一系列反应来制备无水AlCl3。
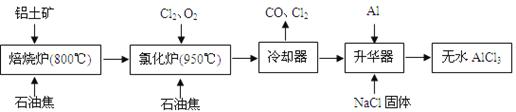
(1)氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则AlCl3是 晶体,其结构式为 。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式是 。
(3)冷却器排出的尾气中含有大量CO和少量Cl2,需用Na2SO3溶液除去Cl2,此反应的离子方程式为: 。
(4)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是: 。
(5)AlCl3产品中Fe元素含量直接影响其品质,为测定产品中Fe元素的含量,现称取16.25g无水AlCl3产品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重残留固体质量为0.32g。则产品中Fe元素的含量为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com