
| ������� | �� | �� | �� | ������ |
| ��ѧʽ | ��HCl ��H2SO4 | ��NaOH ��Ba��OH��2 | ��Na2CO3 ��K2CO3 | ��CO2 ��Na2O2 |
���� ��1���������ʵķ����������Լ�������ĸ�����з��࣬�����Ậ����Ԫ�ز��ܵ���������ӣ���������������ȫ��Ϊ���������ӣ��ε������������Ϊ�������ӣ�������Ϊ������ӣ�S��NΪ�ǽ���Ԫ�أ���Ӧ�ĺ�������H2SO4��H2SO3��HNO3 ��K��NaΪ���ý���Ԫ�أ���Ӧ�ļ���NaOH��KOH���γɵ���Ϊ�������Σ���Na2SO4��K2SO3��K2SO4��NaNO3��KNO3��NaNO2��Na2SO3�ȣ�
��2����Ϊ̼���Σ���Ϊ���������Ϊ������̼��������̼���Ժ�ǿ�Ӧ����̼���Σ�
��3�����ݶ�����̼��ʵ�����Ʒ��ͼ��鷽�����з�����
��� �⣺��1��S��NΪ�ǽ���Ԫ�أ���Ӧ�ĺ�������H2SO4��H2SO3��HNO3 ��K��NaΪ���ý���Ԫ�أ���Ӧ�ļ���NaOH��KOH���γɵ���Ϊ�������Σ���Na2SO4��K2SO3��K2SO4��
�ʴ�Ϊ����H2SO4����NaOH����K2CO3��
��2����Ϊ̼���Σ���Ϊ���������Ϊ������̼��������̼���Ժ�ǿ���������Ʒ�Ӧ����̼���ƺ�ˮ��2NaOH+CO2=Na2CO3+H2O��
�ʴ�Ϊ��2NaOH+CO2�TNa2CO3+H2O��
��3��ʵ�����Ʊ�������̼����ʯ��ʯ��ϡ���ᷴӦ�����������̼�ķ����ǽ�����ͨ������ʯ��ˮ��������ʯ��ˮ����ǣ���֤���������Ƕ�����̼������ʽΪCa��OH��2+CO2�TCaCO3+H2O��
�ʴ�Ϊ��ʯ��ʯ�����Ca��OH��2+CO2�TCaCO3+H2O��
���� �����ۺϿ������ʵķ��ࡢ���ʣ�Ϊ��Ƶ���㣬���ؿ���˫��֪ʶ������������ѧ�����õĿ�ѧ�������ѶȲ���ע�����������ʵ����ʣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
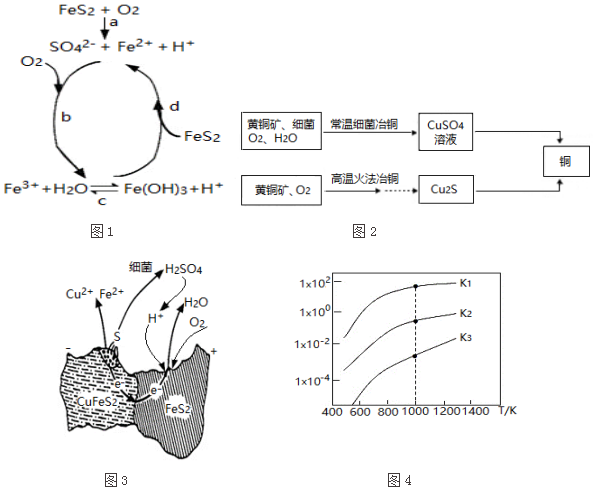
| ��ط�Ӧ | ��Ӧ�� | ƽ�ⳣ�� |
| FeS2��s��+H2��g��?FeS��s��+H2S��g�� | ��H1 | K1 |
| $\frac{1}{2}$FeS2��s��+H2��g��?$\frac{1}{2}$Fe��s��+H2S��g�� | ��H2 | K2 |
| FeS��s��+H2��g��?Fe��s��+H2S��g�� | ��H3 | K3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʽΪC3H6Cl2���л�����4��ͬ���칹�� | |
| B�� | ��װ�ò��Ͼ�����ϩ�����к���̼̼˫�� | |
| C�� | ����Һ���Ϻ�������۷����˼ӳɷ�Ӧ | |
| D�� | 1molƻ���ᣨHOOCCHOHCH2COOH������3molNaHCO3������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2-�������һ�������4�� | |
| B�� | ��ϩ�;�����ϩ����ʹ��ˮ��ɫ | |
| C�� | �Ҵ�������ȿ���NaOH���֣�Ҳ������С�մ����� | |
| D�� | �����������ܷ����ӳɷ�Ӧ���ܷ���ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ����� | �Լ� | ���뷽�� | |
| A | �������ӣ� | ��ˮ | ���� |
| B | ���飨��ϩ�� | ���� | ���� |
| C | �������������ᣩ | NaOH��Һ | ���� |
| D | ���ۣ��Ȼ��ƣ� | ����ˮ | ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �ڢۢ� | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 D�����ڱ���λ�ã���������VIIA�壮
D�����ڱ���λ�ã���������VIIA�壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com