
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | Na2O2中既含有离子键又含有非极性共价键 | |
| C. | KOH中只含有共价键 | |
| D. | KI和HI中化学键类型完全相同 |
分析 金属阳离子和阴离子之间的化学键为离子键,一般盐、碱金属氧化物中含有离子键,非金属元素之间的化学键为共价键,其中相同非金属元素形成的为非极性共价键,不同非金属元素形成的为极性共价键,据此进行判断.
解答 解:A.含有共价键的化合物可能是离子化合物,也可能是共价化合物,如NaOH是离子化合物、HCl是共价化合物,故A错误;
B.Na2O2中钠离子与过氧根离子之间形成离子键,O原子之间形成非极性键,所以既含有离子键又含有非极性共价键,故B正确;
C.KOH中含有离子键和共价键,故C错误;
D.KI只含有离子键,HI只含有共价键,二者的化学键类型不相同,故D错误;
故选B.
点评 本题考查化学键和化合物的关系,侧重考查基本概念,把握物质的构成微粒及化学键的形成条件即可解答,注意离子键和共价键的区别,题目难度不大.


科目:高中化学 来源: 题型:选择题
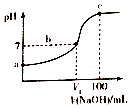 已知某酸HA的电离常数Ka=2.0×10-8,用2mol/LNaOH溶液滴定100ml2mol/LHA溶液,溶液的pH随滴入NaOH溶液的体积变化曲线如图.下列说法正确的是( )
已知某酸HA的电离常数Ka=2.0×10-8,用2mol/LNaOH溶液滴定100ml2mol/LHA溶液,溶液的pH随滴入NaOH溶液的体积变化曲线如图.下列说法正确的是( )| A. | a点溶液的pH=4 | |
| B. | b点溶液中存在:c(A-)>c(Na+)>c(H+)=c(OH-) | |
| C. | b点c(HA)/c(A-)=5 | |
| D. | c点c(A-)+c(H+)=c(Na+)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)3 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 4.7 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4•7H2O | 30.9 | 35.5 | 40.8 | 45.6 | - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝可作胃酸的中和剂 | |
| B. | 绚丽缤纷的烟花中添加了含钾、钙、钠、铜等金属元素的化合物 | |
| C. | SiO2、NaOH、HF三者两两均能反应 | |
| D. | 制备单晶硅的过程中不发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.125mol•L-1•min-1 | B. | 0.100 mol•L-1•s-1 | ||
| C. | 0.200 mol•L-1•min-1 | D. | 0.375 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X:位于元素周期表中的第三周期ⅢA 族 | |
| B. | 元素Y:它的二价阳离子核外电子总数与氖原子相同 | |
| C. | 元素Z:它的原子中M层比L层少2个电子 | |
| D. | 元素W:它的化合物的焰色反应颜色呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
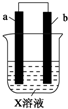 下列对如图所示装置实验现象的描述错误的是( )
下列对如图所示装置实验现象的描述错误的是( ) | a电极 | b电极 | X溶液 | |
| ① | Cu | Zn | CuCl2 |
| ② | Zn | 石墨 | HCl |
| A. | 实验①中a极质量增加 | B. | 实验①中Cl-离子向正极移动 | ||
| C. | 实验②a极质量减少 | D. | 实验②中b极放出无色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol苯分子中含有碳碳双键数为3NA | |
| B. | 常温下,0.1 mol乙烷与乙烯混合气体中所含碳原子数为0.2NA | |
| C. | 14 g乙烯和丙烯的混合气体中所含原子总数为2NA | |
| D. | 标准状况下,22.4 L己烷中共价键数目为19NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com