
同主族常见的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性强弱顺序为:HXO4<HYO4<HZO4,下列判断不正确的是
| A.Y单质可以在海水中提取 | B.离子半径: X->Y- |
| C.气态氢化物稳定性:HX<HZ | D.单质氧化性: Y>Z |
科目:高中化学 来源: 题型:单选题
具有下列电子层结构的原子,其相应元素一定属于同一主族的是
| A.3p轨道上有2个未成对电子的原子和4p轨道上有2个未成对电子的原子 |
| B.3p轨道上只有1个空轨道的原子和4p轨道上只有1个空轨道的原子 |
| C.最外层电子排布为1s2的原子和最外层电子排布为2s22p6的原子 |
| D.最外层电子排布为1s2的原子和最外层电子排布为2s2的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图是元素周期表短周期元素的一部分。已知M最高价氧化物对应的水化物为常见的氧化性酸,下列说法正确的是: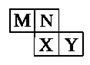
| A.M为氮元素 |
| B.原子半径:Y>X |
| C.氢化物沸点:X>N |
| D.M、X、Y三种元素的最高价氧化物对应的水化物均为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
中学化学中很多“规律”都有其使用范围,下列根据有关“规律”推出的结论合理的是
| A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 |
| B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| C.根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性 |
| D.根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图是元素周期表的一部分,下列说法中正确的是
| A.元素①位于第二周期第ⅣA族 |
| B.气态氢化物的稳定性:④>② |
| C.最高价氧化物对应水化物酸性:⑤>④ |
| D.元素的最高正化合价:③=⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素W、X、Y和Z的原子序数依次增大,金属W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法正确的是
A.由金属W制备的高效电池可用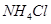 溶液作电解质 溶液作电解质 |
| B.元素Y、Z的最高价氧化物对应水化物之间可以发生反应 |
| C.元素X、Z形成的化合物为离子化合物 |
D.四种元素原子半径由大到小的顺序为: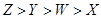 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素M、W、X、Y、Z的原子序数依次增大,M元素的一种核素没有中子,且
M、W、X、Y+、Z的最外层电子数与其电子层数的比值依次为1、2、3、4、2(不考虑零族元素)。下列关于这些元素的叙述正确的是( )
| A.X分别和其它四种元素均可形成至少2种化合物 |
| B.M分别和W、X、Y、Z形成化合物,均显相同化合价 |
| C.M、X、Z三种元素组成的化合物含有离子键 |
| D.M、X、Y组成化合物和Y、Z组成化合物,其等物质的量浓度的水溶液中由水电离出的氢离子浓度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、M、N 代表五种金属。有以下化学反应:
①水溶液中:X+Y2+=X2++Y ②Z+2H2O(冷)=Z(OH)2+H2↑
③M、N 为电极与 N 盐溶液组成原电池,发生的电极反应为:M-2e— =M2+
④Y 可以溶于稀 H2SO4中,M 不被稀 H2SO4氧化. 则这五种金属的活泼性由弱到强的顺序是
| A.M<N<Y<X<Z | B.N<M<X<Y<Z |
| C.N<M<Y<X<Z | D.X<Z<N<M<Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com