
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.使甲基橙变红色的溶液中; K+、Ba2+、AlO2-、NO3-
B.1.0mol/L的KI溶液中: Na+、Fe3+、Cl-、SO42-
C.与铝反应产生大量氢气的溶液中:Mg2+、HCO3-、Cl-、NO3-
D.c(H+)=1×10-13mol/L溶液中:Na+、AlO2-、SiO32-、PO43-
科目:高中化学 来源:2015-2016学年青海省高一下期末化学试卷(解析版) 题型:选择题
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一.对下列实验事实的解释不正确的是( )
现象 | 解释或结论 | |
A | SO2使酸性高锰酸钾溶液退色 | SO2表现还原性 |
B | 浓HNO3在光照条件下变黄 | 浓HNO3不稳定,生成有色产物能溶于浓硝酸 |
C | 某溶液中加入浓NaOH溶液加热,放出气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定含有NH4+ |
D | 铝片放入浓硫酸中,无明显变化 | 说明铝与冷的浓硫酸不发生化学反应 |
A.A B.B C.C D.D
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第二次周测化学试卷(解析版) 题型:填空题
科学家寻找高效催化剂实现大气污染物转化:
2CO(g)+2NO(g) 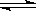 N2(g)+2CO2(g) △H1
N2(g)+2CO2(g) △H1
(1)已知:CO燃烧热△H2=-283kJ·mol-1。几种化学键键能数据如下:
化学键 | N=N键 | O=O键 |
|
键能/kJ·mol-1 | 945 | 498 | 630 |
N2(g)+O2(g)=2NO(g) △H3= ,上述△H1= 。
(2)CO——空气在KOH溶液中构成燃料电池(石墨为电极),若放电后,电解质溶液中离子浓度大小顺序为c(K+)>c(HCO3-)>c(OH-)>c(CO32-)>c(H+),则负极的电极反应式为 。
(3)2CO(g)+2NO(g)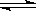 N2(g)+2CO2(g)的平衡常数表达式为 。图A中曲线 (填“I”或“II”)能正确表示平衡常数与温度的关系,理由是 。
N2(g)+2CO2(g)的平衡常数表达式为 。图A中曲线 (填“I”或“II”)能正确表示平衡常数与温度的关系,理由是 。
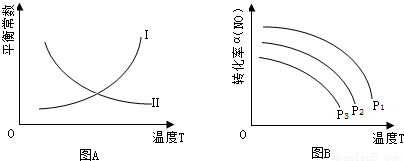
(4)当NO、CO的浓度比为1时,体系中NO平衡转化率(α)与温度、压强的关系如图B所示。α(NO)随着温度升高而 (填“增大”或“减小”),其原因是 。图B中,压强由小到大的顺序为 ,其判断理由是 。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第二次周测化学试卷(解析版) 题型:选择题
有机物M是合成某药品的中间体,结构简式如图所示。下列说法错误的是
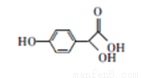
A.用钠可检验M分子中存在羟基
B.M能发生酯化、加成、氧化反应
C.M的分子式为C8H8O4
D.M的苯环上一硝基代物有2种
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第一次月考理综化学试卷(解析版) 题型:填空题
将质量为12.64g KMnO4固体加热一段时间后,收集到amolO2;向反应后残留的固体中加入足量的浓盐酸,又收集到bmolCl2,此时Mn元素全部以Mn2+的形式存在于溶液中。
(1)请完成并配平下列化学方程式:
K2MnO4+ HCl - KCl+ MnCl2+ Cl2↑+________□
该反应中的还原剂是 ,当该反应中转移NA个电子时,氧化产物的物质的量为 mol,被氧化的还原剂的物质的量为 mol。
(2)用酸性高锰酸钾溶液滴定FeSO4溶液写出该反应的离子方程式 。
(3)当KMnO4固体加热生成O2 a mol值最大时,向反应后残留的固体中加入足量的浓盐酸并加热,产生Cl2的物质的量b= mol。(此时Mn元素全部以Mn2+的形式存在于溶液中)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:填空题
金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g) W (s) + 3H2O (g)。请回答下列问题:
W (s) + 3H2O (g)。请回答下列问题:
(1)上述反应的化学平衡常数表达式为____________________。
(2) 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为___________;随温度的升高,H2与水蒸气的体积比减小,则该反应为 反应(填“吸热”或“放热”)。
(3)用H2还原WO2也可得到金属钨。已知:
WO2 (s) + 2H2 (g) W (s) + 2H2O (g) ΔH = +66.0 kJ·mol–1
W (s) + 2H2O (g) ΔH = +66.0 kJ·mol–1
WO2 (g) + 2H2 (g) W (s) + 2H2O (g) ΔH =-137.9 kJ·mol–1
W (s) + 2H2O (g) ΔH =-137.9 kJ·mol–1
则WO2 (s) WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g)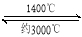 WI4 (g)。下列说法正确的有________(填序号)。
WI4 (g)。下列说法正确的有________(填序号)。
a.灯管内的I2可循环使用 b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
有关键能数据如表所示:已知N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ•mol﹣1.则x的值为( )
化学键 | N≡N | H﹣H | H﹣N |
键能/kJ•mol﹣1 | x | 436 | 391 |
A.945.6 B.649 C.431 D.869
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
在一个不传热的固定容积的密闭容器中可逆反应mA(g)+ nB(g)? pC(g)+ qQ(g) 当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变 ②体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变⑤反应速率v(A):v(B):v(C):v(D)=m:n:p:q
⑥单位时间内m mol A断键反应,同时pmol C也断键反应.
A.③④⑤⑥ B.②③④⑥ C.①③④⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省揭阳市高二期末统考理综化学试卷(解析版) 题型:推断题
[化学——选修5有机化学基础]
M是一种重要材料的中间体,结构简式为: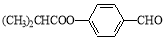 。合成M的一种途径如下:
。合成M的一种途径如下:
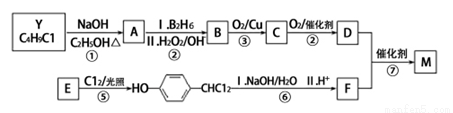
A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:①Y的核磁共振氢谱只有1种峰;
②RCH=CH2 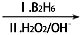 RCH2CH2OH;
RCH2CH2OH;
③两个羟基连接在同一个碳原子上不稳定,易脱水。
请回答下列问题:
(1)D中官能团的名称是 ,Y的结构简式是 。
(2)步骤①的反应类型是 。
(3)下列说法不正确的是 。
a.A和E都能发生氧化反应 b.1 molB完全燃烧需6 mol O2
c.C能与新制氢氧化铜悬浊液反应 d.1 molF最多能与3 mol H2反应
(4)步骤⑦的化学反应方程式是 。
(5)M经催化氧化得到X(C11H12O4),X的同分异构体中同时满足下列条件的结构简为 。
a.苯环上只有两个取代基,苯环上的一氯代物有2种
b.水解只生成芳香醇和二元酸,且二元酸的核磁共振氢谱只有2种峰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com