
| A.SO2气体的还原性较强,不能使其通过浓硫酸干燥 |
| B.滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 |
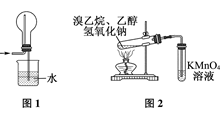
| C.用图1装置吸收多余的HCl气体 |
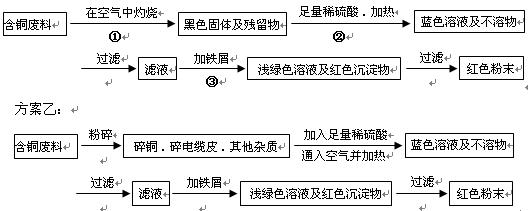
| D.用图2装置检验溴乙烷发生消去反应生成乙烯 |
科目:高中化学 来源:不详 题型:实验题
 __________________ _ __________
__________________ _ __________| 序号 | 实验操作 | 实验现象 | 结论及离子方程式 |
| ① | 取适量的样品于试管内 | —— | —— |
| ② | 用滴管滴入足量硫酸溶液,并充分振荡试管 | | |
| ③ | | 溶液先黄色,滴入KSCN溶液后显红色 | |
| | | | |
 师的建议完成上面操作步骤,获得晶体后对其进行检测
师的建议完成上面操作步骤,获得晶体后对其进行检测查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
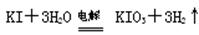
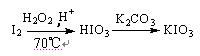
 I2+2S2O32-=2I-+S4O62-。为测定加碘食盐中碘的含量,设计的方案如下。请完善实验步骤并计算测定结果:
I2+2S2O32-=2I-+S4O62-。为测定加碘食盐中碘的含量,设计的方案如下。请完善实验步骤并计算测定结果:| 滴定次数 | 盛标准Na2S2O3溶液的读数 | |
| 滴定前刻度(/mL) | 滴定后刻度(/mL) | |
| 1 | 1.02 | 11.03 |
| 2 | 2.00 | 11.99 |
| 3 | 0.20 | 10.20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾—淀粉试纸检验,观察试纸颜色的变化 |
| B.用核磁共振氢谱图鉴别1-丙醇和2-丙醇 |
| C.测氯水的pH,可用玻璃棒蘸取氯水点在pH试红上,待其变色后和标准比色卡比较 |
| D.铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,铝热剂一定不含Fe2O3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
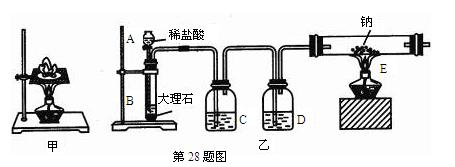
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
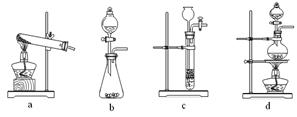
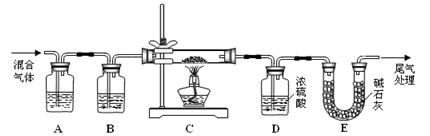
 到干燥、纯净的CO气体,洗气瓶A、B中盛放的试剂分别是 、 。
到干燥、纯净的CO气体,洗气瓶A、B中盛放的试剂分别是 、 。| 实验 编号 | 实验目的 | T/K | 催化剂用量/g | C/mol·l-1:] | |
| KMnO4 | H2C2O4 | ||||
| ① | 为以下实验作参考 | 298 | 0.5 | 0.01 | 0.1 |
| ② | 探究KMnO4酸性溶液的浓度对该反应速率的影响 | 298 | 0.5 | 0.001 | 0.1 |
| ③ | | 323 | 0.5 | 0.01 | 0.1 |
| ④ | 探究催化剂对反应速率的影响 | | | | 0.1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
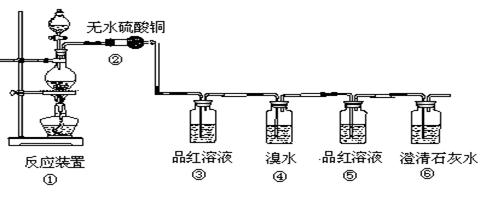
 漏气。
漏气。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.100 mL烧杯 | B.500 mL容量瓶 | C.玻璃棒 | D.100 mL容量瓶 E、漏斗 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
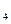 和C
和C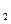 H
H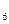 的比例关系,设计实验如下图所示:
的比例关系,设计实验如下图所示: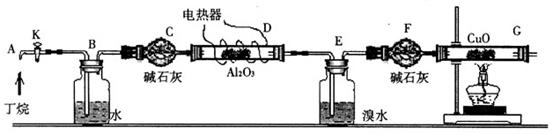
 D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等……
D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等……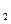 和H
和H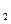 O;A
O;A l
l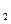 O
O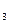 是烷烃裂解的催化剂;G后面装置已省略。
是烷烃裂解的催化剂;G后面装置已省略。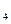 和C
和C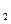 H
H

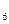 的物质的量之比n(CH
的物质的量之比n(CH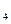 ):n(C
):n(C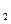 H
H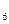 )=______________。
)=______________。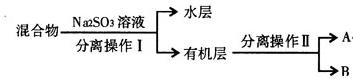

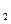 SO
SO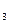 溶液的作用是______________________。
溶液的作用是______________________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com