
从下列事实所得出的相应结论正确的是( )
| 实验事实 | 结论 |
① | 在相同温度下,向1 mL 0.2 mol·L-1 NaOH溶液中滴入2滴0.1 mol·L-1 MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol·L-1 FeCl3溶液,又生成红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
② | 将CO2通入到Na2SiO3溶液中产生白色浑浊 | 酸性:H2CO3>H2SiO3 |
③ | 已知反应5Cl2+I2+6H2O=2HIO3+10HCl,2BrO3-+Cl2=2ClO3-+Br2 | 氧化性强弱顺序:BrO3->Cl2>ClO3->IO3- |
④ | 测定等物质的量浓度的Na2SO4与Na2CO3溶液的pH,后者较大 | 非金属性:S>C |
A.③④ B.②④ C.①②③ D.全部
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-1练习卷(解析版) 题型:选择题
某无色溶液中含有大量Na2SO4、Na2CO3、NaOH,为验证其中所含的阴离子,若限定只取一次待测液,则加入试剂顺序正确的是( )
A.酚酞、BaCl2、盐酸 B.BaCl2、盐酸、酚酞
C.BaCl2、酚酞、盐酸 D.酚酞、盐酸、BaCl2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十四 定量计算型专题练习卷(解析版) 题型:选择题
将一定量的氯气通入30 mL浓度为10.00 mol·L-1的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是( )
A.与NaOH反应的氯气一定为0.3 mol
B.n(Na+)∶n(Cl-)可能为7∶3
C.若反应中转移的电子为n mol,则0.15<n<0.25
D.n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十二 仪器组合型专题练习卷(解析版) 题型:选择题
下列关于各实验装置图的叙述中正确的是( )
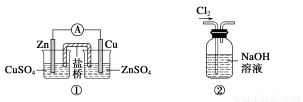
A.装置①:构成锌—铜原电池
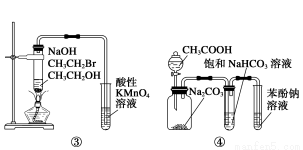
B.装置②:除去Cl2中含有的少量HCl
C.装置③:验证溴乙烷发生消去反应生成烯烃
D.装置④:由实验现象推知酸性强弱顺序为CH3COOH>H2CO3>C6H5OH
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十二 仪器组合型专题练习卷(解析版) 题型:选择题
下图所示的实验装置不能完成实验目的是( )
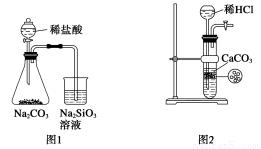
A.图1为证明非金属性强弱:Cl>C>Si
B.图2为制备少量CO2并控制反应
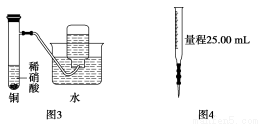
C.图3为制备并收集少量NO气体
D.图4量取0.10 mol·L-1 KOH溶液20.00 mL
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十三 表格实验型专题练习卷(解析版) 题型:选择题
下列实验不能达到预期实验目的的是( )
序号实验内容实验目的
A向盛有10滴0.1 mol·L-1 AgNO3溶液的试管中滴加0.1 mol·L-1 NaCl溶液,至不再有沉淀生成,再向其中滴加0.1 mol·L-1 Na2S溶液 证明AgCl能转化为溶解度更小的Ag2S
B向2 mL甲苯中加入3滴酸性KMnO4溶液,振荡;向2 mL苯中加入3滴酸性KMnO4溶液,振荡 证明与苯环相连的甲基易被氧化
C向Na2SiO3溶液中通入CO2证明碳酸的酸性比硅酸强
D向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜悬浊液并加热 验证淀粉已水解
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十一 图像分析型专题练习卷(解析版) 题型:选择题
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表。以下推断正确的是( )
氢氧化物 | 溶液pH | |||
开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.4 | - | - |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
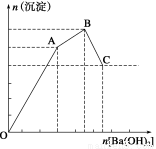
A.C点的沉淀为Fe(OH)3
B.OA段可能发生的反应有:3Ba2++6OH-+3SO42-+2Fe3+=3BaSO4↓+2Fe(OH)3↓
C.AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-=2BaSO4↓+Al(OH)3↓
D.据图计算原溶液中c(Cl-)>c(SO42-)
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型十 粒子变化型专题练习卷(解析版) 题型:选择题
常温下,有下列四种溶液:
① | ② | ③ | ④ |
0.1 mol·L-1NaOH溶液 | pH=11 NaOH溶液 | 0.1mol·L-1 CH3COOH溶液 | pH=3 CH3COOH溶液 |
下列说法正确的是( )
A.由水电离出的c(H+):①>③
B.③稀释到原来的100倍后,pH与④相同
C.②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D.①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2014年高考化学 题型五 物质结构型专题练习卷(解析版) 题型:选择题
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是( )
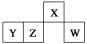
A.原子半径:rW>rZ>rY>rX
B.含Y元素的盐溶液显酸性
C.最简单气态氢化物的热稳定性:Z>W
D.X与氢元素组成的化合物XH5与水反应可产生两种气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com