
| A£® | ĘäĖ®ČÜŅŗĻŌĒæĖįŠŌ£¬Ė×³ĘŹÆĢæĖį | |
| B£® | ĘäÅØČÜŅŗ¶Ōʤ·ōÓŠĒæĮŅµÄøÆŹ“ŠŌ£¬Čē¹ū²»É÷Õ“ŌŚĘ¤·ōÉĻ£¬Ó¦Į¢¼“ÓĆ¾Ę¾«²ĮĻ“ | |
| C£® | ĘäŌŚĖ®ÖŠµÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ųŌö“󣬳¬¹ż65”ęæÉŅŌÓėĖ®ŅŌČĪŅā±Č»„ČÜ | |
| D£® | ĀČ»ÆĢśČÜŅŗÖŠµĪČė±½·ÓµÄĖ®ČÜŅŗŗó£¬ČÜŅŗ³Ź×ĻÉ« |
·ÖĪö A£®±½·ÓÖŠ·ÓōĒ»łÄܲæ·ÖµēĄė³öĒāĄė×Ó¶ųµ¼ÖĀČÜŅŗ³ŹĖįŠŌ£»
B£®±½·ÓÓŠøÆŹ“ŠŌ£¬µ«Ņ×ČÜÓŚ¾Ę¾«£»
C£®±½·ÓŌŚ³¬¹ż65”ęæÉŅŌÓėĖ®ŅŌČĪŅā±Č»„ČÜ£»
D£®ĀČ»ÆĢśŗĶ±½·Ó·“Ó¦·¢ÉśĻŌÉ«·“Ó¦£®
½ā“š ½ā£ŗA£®±½·ÓÖŠ·ÓōĒ»łÄܲæ·ÖµēĄė³öĒāĄė×Ó¶ųµ¼ÖĀČÜŅŗ³ŹĖįŠŌ£¬ŅņĪŖ²æ·ÖµēĄė¶ųŹ¹ČÜŅŗ³ŹČõĖįŠŌ£¬Ė×³ĘŹÆĢæĖį£¬¹ŹA“ķĪó£»
B£®±½·ÓÓŠøÆŹ“ŠŌ£¬µ«Ņ×ČÜÓŚ¾Ę¾«£¬ĖłŅŌĘäÅØČÜŅŗ¶Ōʤ·ōÓŠĒæĮŅµÄøÆŹ“ŠŌ£¬Čē¹ū²»É÷Õ“ŌŚĘ¤·ōÉĻ£¬Ó¦Į¢¼“ÓĆ¾Ę¾«²ĮĻ“£¬¹ŹBÕżČ·£»
C£®±½·ÓŌŚĖ®ÖŠµÄČܽā¶ČĖęĪĀ¶ČµÄÉżø߶ųŌö“ó£¬æÉŅŌŗĶĖ®ŠĪ³É·Ö×Ó¼äĒā¼ü£¬³¬¹ż65”ęæÉŅŌÓėĖ®ŅŌČĪŅā±Č»„ČÜ£¬¹ŹCÕżČ·£»
D£®ĀČ»ÆĢśŗĶ±½·Ó·“Ó¦·¢ÉśĻŌÉ«·“Ó¦¶ųŹ¹ĀČ»ÆĢśČÜŅŗ³Ź×ĻÉ«£¬øĆĻÖĻóæÉŅŌ¼ģŃé±½·Ó£¬¹ŹDÕżČ·£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģā漲鱽·ÓŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬×¢Ņā·ÓŗĶ“¼ÖŠ¶¼ŗ¬ÓŠ-OH£¬µ«¶žĄąĪļÖŹŠŌÖŹ²»Ķ¬£¬Ö»ÓŠ-OHÖ±½ÓĮ¬½Ó±½»·Ź±²ÅŹĒ·Ó£¬×¢Ņā±½·ÓµÄĢŲÕ÷·“Ó¦£¬ĢāÄæÄŃ¶Č²»“ó£®


 ÖĒ»ŪæĪĢĆĆܾķ100·Öµ„ŌŖ¹ż¹Ų¼ģ²āĻµĮŠ“š°ø
ÖĒ»ŪæĪĢĆĆܾķ100·Öµ„ŌŖ¹ż¹Ų¼ģ²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
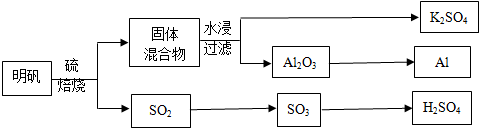

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | õ„ĄąĪļÖŹŹĒŠĪ³ÉĖ®¹ūĻćĪ¶µÄÖ÷ŅŖ³É·Ö | |
| B£® | ĢĒĄąĪļÖŹ¶¼¾ßÓŠĻąĶ¬µÄ¹ŁÄÜĶÅ | |
| C£® | ÓĶÖ¬µÄŌķ»Æ·“Ӧɜ³Éøß¼¶Ö¬·¾ĖįŗĶøŹÓĶ | |
| D£® | µ°°×ÖŹµÄĖ®½ā²śĪļ¶¼ŗ¬ÓŠōČ»łŗĶōĒ»ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ąė×Ó»ÆŗĻĪļæÉÄÜŗ¬ÓŠ¹²¼Ū¼ü | B£® | ¹²¼Ū»ÆŗĻĪļæÉÄÜŗ¬ÓŠĄė×Ó¼ü | ||
| C£® | Ąė×Ó»ÆŗĻĪļÖ»ŗ¬ÓŠĄė×Ó¼ü | D£® | ŅŌÉĻĖµ·Ø¾ł²»ÕżČ· |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H3PO4?3H++PO43- | B£® | BaSO4?Ba2++SO42- | ||
| C£® | Al£ØOH£©3?H2O+AlO2-+H+ | D£® | NaHS?Na++H++S2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
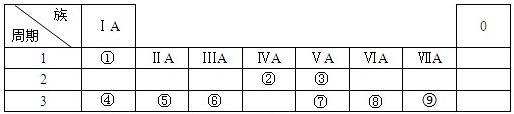
 £»ŌŖĖŲµÄ¢įĄė×Ó½į¹¹Ź¾ŅāĶ¼ŹĒ
£»ŌŖĖŲµÄ¢įĄė×Ó½į¹¹Ź¾ŅāĶ¼ŹĒ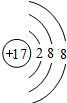 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žŃõ»ÆĀČŹĒĒæŃõ»Æ¼Į | B£® | ¶žŃõ»ÆĀČŹĒĒ滹Ō¼Į | ||
| C£® | ¶žŃõ»ÆĀČŹĒµē½āÖŹ | D£® | ¶žŃõ»ÆĀČ·Ö×ÓÖŠĀČĪŖ-1¼Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2SO3µÄĖįŠŌ±ČH2CO3µÄĖįŠŌĒ棬ĖµĆ÷SµÄ·Ē½šŹōŠŌ±ČCĒæ | |
| B£® | øł¾Ż·Ē½šŹōŠŌĒæČõF£¾Cl£¬æÉŅŌĶĘ²ā·ŠµćHF£¾HCl | |
| C£® | ½ųŠŠH2OŗĶH2SĘųĢåµÄČČ·Ö½āŹµŃ飬æÉČ·¶ØS”¢OĮ½ÖÖŌŖĖŲµÄ·Ē½šŹōŠŌĒæČõ | |
| D£® | ŅŃÖŖ2C+SiO2$\frac{\underline{\;øßĪĀ\;}}{\;}$Si+2CO”ü£¬ĖµĆ÷CµÄ·Ē½šŹōŠŌ±ČSiĒæ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com