
| A. | 在稀盐酸中:Ba2+、CO32-、Zn2+ | B. | 在氢氧化钠溶液中:H+、Mg2+、Cl- | ||
| C. | 在硫酸铵溶液中:Na+、K+、OH- | D. | 在氯化钠溶液中:K+、Ca2+、N03- |
分析 A.钡离子、锌离子与碳酸根离子反应,且碳酸根离子与稀盐酸中的氢离子反应;
B.镁离子、氢离子与氢氧化钠反应;
C.氢氧根离子与硫酸铵电离出的铵根离子反应;
D.三种离子之间不发生反应,都不与氯化钠反应.
解答 解:A.CO32-与Ba2+、Zn2+之间发生反应,CO32-与稀盐酸反应,在溶液中不能大量共存,故A错误;
B.H+、Mg2+与氢氧化钠发生反应,在溶液中不能大量共存,故B错误;
C.硫酸铵电离出铵根离子,OH-与铵根离子发生反应生成一水合氨,在溶液中不能大量共存,故C错误;
D.K+、Ca2+、N03-之间不反应,都不与氯化钠反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存,题目难度中等,明确离子反应发生条件为解答关键,注意掌握离子共存的条件及判断方法,还要注意题干暗含条件,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题


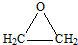 .
.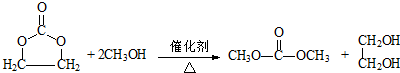 .
.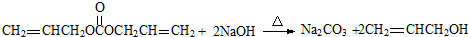 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯在催化剂作用下能与溴水发生取代反应 | |
| B. | 实验室用CaC2和饱和食盐水制备乙炔 | |
| C. | 氯乙烷在氢氧化钠的水溶液中生成乙烯 | |
| D. | 将苯、浓HNO3的混合物用水浴加热(60℃左右)制备硝基苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
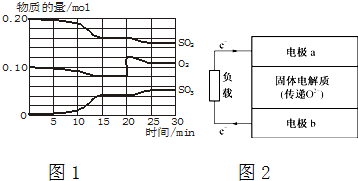
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于24s | B. | 等于20s | C. | 大于20s | D. | 小于20s |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学实验小组需要2mol•L-1的NaCl溶液98ml,现用NaCl固体来配制,请回答下列问题:
某化学实验小组需要2mol•L-1的NaCl溶液98ml,现用NaCl固体来配制,请回答下列问题: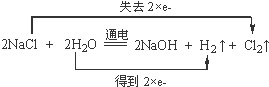 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
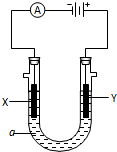
 如图,A池用石墨电极电解饱和KCl溶液,B池精炼粗铜,当d极产生具有氧化性的气体在标准状况下为2.24L时停止通电,此时A池中KCl有剩余且溶液的体积为200mL,下列说法正确的是( )
如图,A池用石墨电极电解饱和KCl溶液,B池精炼粗铜,当d极产生具有氧化性的气体在标准状况下为2.24L时停止通电,此时A池中KCl有剩余且溶液的体积为200mL,下列说法正确的是( )| A. | 向A池中通入4.48 L HCl气体可恢复到电解前的状态 | |
| B. | 停止通电后恢复至室温A池中溶液的pH值为14 | |
| C. | 电极e应为粗铜板材料且质量减少6.4 g | |
| D. | 该电路中通过的电子的物质的量为0.4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
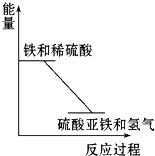 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势,如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 | |
| B. | 除去甲烷气体中的乙烯可以将混合气体通过盛有足量酸性高锰酸钾溶液的洗气瓶 | |
| C. | 苯的二氯代物有3种,说明苯分子是由6个碳原子以单双键交替结合而成的六元环 | |
| D. | 乙酸和乙醇在浓硫酸作用下可以反应,该反应属于加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com