
【题目】二茂铁[(C5H5)2Fe]分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如图所示,下列说法不正确的是( )

A. 二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为配位键
B. lmol环戊二烯(![]() )中含有
)中含有![]() 键的数目为11NA
键的数目为11NA
C. 二茂铁分子中存在π键
D. Fe2+的电子排布式为ls 22s 22p63s23p63d44s2
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
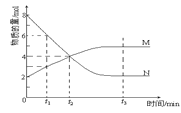
A.反应的化学方程式:2M![]() N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:

(1)A的结构式为 ________________;C的结构简式为_________________;
(2)写出反应①的化学方程式_________________;
(3)反应③的反应类型为__________________;
(4)C通常有三种不同类别的芳香族同分异构体,试写出另两种不同类别的同分异构体的结构简式(各写一种)______________;_______________。
(5)反应 ________(填序号)原子的理论利用率为100%,符合绿色化学的要求。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法不正确的是( )
A.向0.1mol·L-1 CH3COONa溶液中加入少量水,溶液中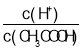 减小
减小
B.将FeCl3溶液和Fe2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分不同
C.向盐酸中加入氨水至中性,溶液中![]() =1
=1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)镍与CO反应会造成镍催化剂中毒。为防止镍催化剂中毒,工业上常用SO2除CO。已知:
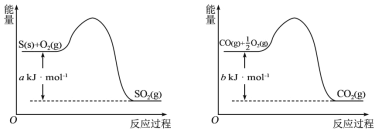
则用SO2除去CO的热化学方程式为___。
(2)含乙酸钠和对氯酚(![]() )的废水可以利用微生物电池除去,其原理如图所示:
)的废水可以利用微生物电池除去,其原理如图所示:
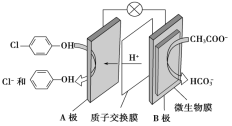
①B是电池的___极(填“正”或“负”);
②A极的电极反应式为____。
(3)利用双模三室电解法不仅可处理含NiCl2的废水,还可回收金属镍,其装置如图所示。
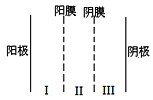
①两端电解质溶液分别为含NiCl2的废水和NaOH溶液,其中含NiCl2的废水应进___(填“Ⅰ”“Ⅱ”“Ⅲ”,下同)室。
②阳极的电极反应式为___。
(4)某研究性学习小组根据反应2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1mol·L-1,溶液的体积均为200mL,盐桥中装有饱和K2SO4溶液。
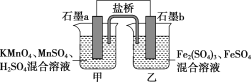
回答下列问题:
①此原电池的正极是石墨___(填“a”或“b”),发生___反应。
②电池工作时,盐桥中的SO42-移向____(填“甲”或“乙”)烧杯。
③甲烧杯中的电极反应式为____;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素。
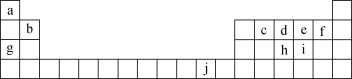
回答下列问题:
(1)写出元素f的基态原子核外电子排布式:____。
(2)写出元素h的基态原子核外电子轨道表示式:________。
(3)基态b原子电子占据最高能级的电子云轮廓图为_________
(4)ce2分子的电子式为____。
(5)d、g、h的原子半径由小到大的顺序是_______(用元素符号表示)
(6)用一个化学方程式证明e、i的非金属性的强弱_________。
(7)d的简单氢化物比h的简单氢化物沸点____(填“高”或“低”),请分析其原因____,写出j的原子结构示意图_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型漂白剂(结构如图)可用于漂白羊毛、草等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
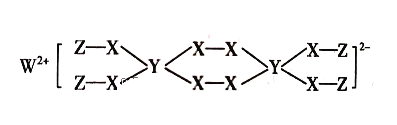
A.元素电负性顺序为:X>W>Y
B.Y的最高价氧化物对应水化物为强酸
C.工业上通过电解熔融的WX来制得W
D.该漂白剂中X、Y均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常用于制造医药品,染料等。某化学小组在实验室利用纯净干燥的氯气和二氧化硫反应制取硫酰氯,所需实验装置如图所示(部分装置略)。
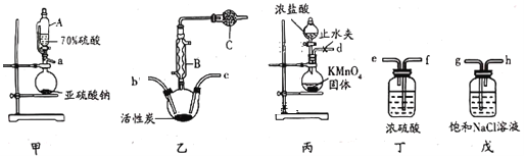
已知:①硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿的空气中“发烟”;
②SO2(g)+Cl2(g)=SO2Cl2(l),△H=-97.3kJ/mol。
(1)仪器A为恒压分液漏斗,与普通分液漏斗相比,其优点是___;仪器B的名称是___。
(2)上述装置的连接顺序:a接 , 接 , 接 , 接 , 接d。(装置可以重复使用)___
(3)球形干燥管C中的试剂为___,作用为___。
(4)硫酰氯在潮湿空气中“发烟”的原因是___(用化学方程式表示)
(5)在无活性炭存在的条件下SO2与Cl2也可发生反应,现将SO2、Cl2按照一定比例通入水中,请设计一个最简单的实验方案验证二者是否恰好完全反应:____。(简要描述实验操作,现象和结论)仪器自选,可供选择的试剂:酸性高锰酸钾溶液、碘化钾溶液、淀粉溶液、品红溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种线性高分子,结构如下图所示。
![]()
下列有关说法正确的是( )
A. 该高分子由4种单体缩聚而成
B. 构成该高分子的单体中有2种羧酸
C. 上述单体中的乙二醇,可被O2催化氧化生成单体之一的草酸
D. 该高分子有固定熔、沸点,1 mol上述链节完全水解需要氢氧化钠物质的量为 5 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com