
三颈瓶在化学实验中的应用非常广泛,下面是三颈瓶在部分无机实验或有机实验中的一些应用。
(1)在如图所示装置中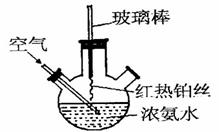 ,进行氨的催化氧化实验:向三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶子并接近液面。反应过程中可观察到瓶中有红棕色气体产生,铂丝始终保持红热。实验过程中
,进行氨的催化氧化实验:向三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶子并接近液面。反应过程中可观察到瓶中有红棕色气体产生,铂丝始终保持红热。实验过程中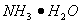 的电离程度____(填“变大”、“变小”或“不变”)
的电离程度____(填“变大”、“变小”或“不变”)
(2)实验室用下图所示装置制备氨基甲酸铵(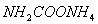 ),其反应化学方程式:
),其反应化学方程式:
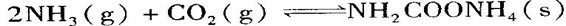
该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
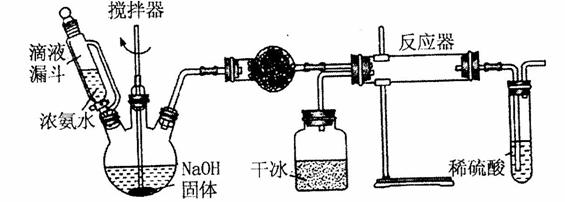
①写出加入药品之前实验操作的要点_______;反应中若有水存在则生成碳酸氢铵的化学方程式是________________________。
②干燥管中盛放的药品是______。简述左侧三颈瓶装置制取氨气的原理________。
③对比碳酸盐和酸的反应制取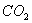 ,该实验利用干冰升华产生
,该实验利用干冰升华产生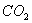 气体的有优点有_____.
气体的有优点有_____.
④有同学认为该实验装置存在安全问题,请问可能面临的安全问题是________。
⑤氨基甲酸氨可用作肥料,其肥效比尿素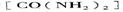 _______(填“高”或“低”),在潮湿的空气中释放出氨而变成碳酸氢铵。取因部分变质二混有碳酸氢铵的氨基甲酸铵样品0.7830g,用足量石灰水充分处理后,使样品中碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g,则样品中氨基甲酸铵的物质的量分数是_____________。
_______(填“高”或“低”),在潮湿的空气中释放出氨而变成碳酸氢铵。取因部分变质二混有碳酸氢铵的氨基甲酸铵样品0.7830g,用足量石灰水充分处理后,使样品中碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g,则样品中氨基甲酸铵的物质的量分数是_____________。
科目:高中化学 来源: 题型:
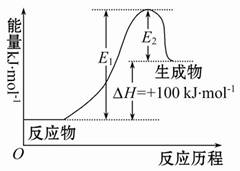
某反应的ΔH=+100 kJ·mol-1,下列有关该反应的叙述正确的是( )
A.正反应活化能小于100 kJ·mol-1
B.逆反应活化能一定小于100 kJ·mol-1
C.正反应活化能不小于100 kJ·mol-1
D.正反应活化能比逆反应活化能大100 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是:
A. 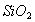 是酸性氧化物,能与溶液反应
是酸性氧化物,能与溶液反应
B. 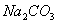 和
和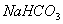 都是盐,都能与溶液反应
都是盐,都能与溶液反应
C.  和
和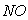 都是大气污染物,在空气中都能稳定存在
都是大气污染物,在空气中都能稳定存在
D. Al在浓盐酸中会“钝化”,能用铝槽盛放浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,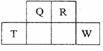 其中T所处的周期序数与主族序数相等。
其中T所处的周期序数与主族序数相等。
(1)T的原子结构示意图是_______。用化学方程式表示冶炼T单质常用原理是________。
(2)与同主族的某元素,其氢氧化物分子含有18个电子,该分子中存在的共价键的类型是___________。
(3)元素的非金属性:Q___W(填“强于”或“弱于”),用方程式简述其理由______。
(4)甲是R的氧化物,通常状况下呈红棕色。现有一试管甲,欲使元素R全部转化为其最高价氧化物对应水化物。实验步骤:将盛有甲的试管倒扣在水槽中,____。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1。则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
B.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)====2CO(g)+O2(g)反应的ΔH=+2×283.0 kJ·mol-1
C.C2H6的燃烧热为Q kJ·mol-1,则表示C2H6燃烧热的热化学方程式为2C2H6(g)+7O2(g)====4CO2(g)+6H2O(l) ΔH=-2Q kJ·mol-1
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,用甲烷制备合成气的反应为:
①CH4(g)+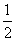 O2(g)====CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
O2(g)====CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
②CH4(g)+H2O(g)====CO(g)+3H2(g) ΔH2=+216 kJ·mol-1
(1)氢气与氧气反应生成水蒸气的热化学方程式为
___________________________________________________________________。
(2)现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
①若x=0.2,反应①放出的能量为________ kJ。
②若x=0.5,反应①与②______(填“放出”或“吸收”)的总能量为_____kJ。
③若x=________时,反应①与②放出(或吸收)的总能量为0。
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数为Z的元素R,在元素周期表中位于A、B、C、D四种元素的中间,A、B、C、D四种元素的原子序数之和为下列数据,其中不可能的是 ( )
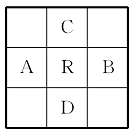
A.4Z B.4Z+10
C.4Z+5 D.4Z+14
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
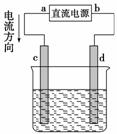
A.a为负极,b为正极
B.a为阳极,b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com