
ЁОЬтФПЁПЯТБэЮЊдЊЫижмЦкБэЕФвЛВПЗжЃЌЧыВЮеедЊЫиЂйЁЋЂрдкБэжаЕФЮЛжУЃЌЛиД№ЯТСаЮЪЬтЃК
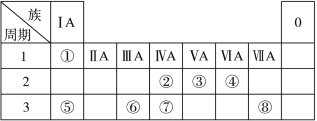
ЃЈ1ЃЉЕиПЧжаКЌСПзюИпЕФН№ЪєдЊЫидкжмЦкБэжаЕФЮЛжУЪЧ ЁЃ
ЃЈ2ЃЉЂраЮГЩЕФЕЅжЪгыЫЎЗДгІЕФРызгЗНГЬЪНЮЊ ЁЃ
ЃЈ3ЃЉЂкЂпЕФЗЧН№ЪєадЧПШѕПЩЭЈЙ§БШНЯетСНжждЊЫи (ЬюБрКХ)
aЃЎдзгЕФЕУЕчзгЕФФмСІ
bЃЎКЌбѕЫсЕФЫсад
cЃЎЦјЬЌЧтЛЏЮяЕФЮШЖЈад
dЃЎЕЅжЪЕФШлЗаЕу
ЃЈ4ЃЉаДГівЛжжгЩЂмЂнЂрдЊЫиаЮГЩЕФМШКЌгаРызгМќгжКЌгаЙВМлМќЕФЮяжЪЕФЕчзгЪН ЁЃ
ЃЈ5ЃЉЛЏЙЄаавЕзюНќКЯГЩСЫгЩдЊЫиЂкКЭЂлаЮГЩЕФЛЏКЯЮяЃЌЦфгВЖШБШН№ИеЪЏЛЙДѓЁЃИУЮяжЪЫљаЮГЩЕФОЇЬхЛЙПЩФмОпгаЕФаджЪЛђЬиЕуга (ЬюБрКХ)
ЂйШлЕуКмИп
ЂкПЩвдЕМЕч
ЂлВЛДцдкЕЅИіЗжзг
ЂмОпгаПеМфЭјзДНсЙЙ
ЃЈ6ЃЉЂйКЭЂлаЮГЩЕФФГвКЬЌЛЏКЯЮяФІЖћжЪСПгыбѕЦјЯрЭЌЁЃдкГЃЮТГЃбЙЯТ0.25 molИУвКЬЌЮяжЪдкзуСПЕФбѕЦјжаЭъШЋШМЩеЩњГЩЂлЕФЦјЬЌЕЅжЪКЭвКЬЌЫЎЃЌЭЌЪБЗХГіQkJЕФШШСПЁЃаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН____________________________ ______ЁЃ
ЁОД№АИЁПЃЈ1ЃЉЕк3жмЦк ЂѓAзх
ЃЈ2ЃЉCl2ЃЋH2O![]() HClOЃЋHЃЋЃЋClЃ
HClOЃЋHЃЋЃЋClЃ
ЃЈ3ЃЉa c(ЩйбЁЕУ1ЗжЃЌДэбЁВЛЕУЗж)
ЃЈ4ЃЉ![]() Лђ
Лђ![]()
ЃЈ5ЃЉЂй Ђл Ђм
ЃЈ6ЃЉN2H4(l)ЃЋO2(g) = N2(g)ЃЋ2H2O(l) H=" ЁЊ4Q" kJЁЄmolЃ1
ЁОНтЮіЁПЪдЬтЗжЮіЃКЃЈ1ЃЉЕиПЧжаКЌСПзюИпЕФН№ЪєдЊЫиЮЊТСдЊЫиЃЌдкжмЦкБэжаЕФЮЛжУЪЧЕк3жмЦкЂѓAзхЁЃ
ЃЈ2ЃЉЂрЮЊТШдЊЫиЃЌТШЦјгыЫЎЗДгІЩњГЩбЮЫсКЭДЮТШЫсЃЌРызгЗНГЬЪНЮЊCl2ЃЋH2O![]() HClOЃЋHЃЋЃЋClЃЁЃ
HClOЃЋHЃЋЃЋClЃЁЃ
ЃЈ3ЃЉЂкЮЊЬМдЊЫиЃЌЂпЮЊЙшдЊЫиЃЌЗЧН№ЪєадЧПШѕПЩЭЈЙ§БШНЯдзгЕФЕУЕчзгЕФФмСІЁЂЕЅжЪгыЧтЛЏКЯЕФФбвзМАЦјЬЌЧтЛЏЮяЕФЮШЖЈадЁЂзюИпМлбѕЛЏЮяЫЎЛЏЮяЕФЫсадНјааБШНЯЃЌбЁaЁЂcЁЃ
ЃЈ4ЃЉЂмЮЊбѕдЊЫиЃЌЂнЮЊФЦдЊЫиЃЌЂрЮЊТШдЊЫиЃЌШ§епаЮГЩЕФМШКЌгаРызгМќгжКЌгаЙВМлМќЕФЮяжЪЮЊДЮТШЫсФЦЃЌЕчзгЪНЮЊ![]() Лђ
Лђ![]() ЁЃ
ЁЃ
ЃЈ5ЃЉЂкЮЊЬМдЊЫиЃЌЂлЮЊЕЊдЊЫиЃЌИљОнЬтвтжЊЖўепаЮГЩЕФЛЏКЯЮяЮЊдзгОЇЬхЃЌОпгагВЖШДѓЃЌШлЕуИпЃЌВЛДцдкЕЅИіЗжзгЃЌОпгаПеМфЭјзДНсЙЙЕШЃЌбЁЂйЂлЂмЁЃ
ЃЈ6ЃЉЂйЮЊЧтдЊЫиЃЌЂлЮЊЕЊдЊЫиЃЌЖўепаЮГЩЕФФГвКЬЌЛЏКЯЮяФІЖћжЪСПгыбѕЦјЯрЭЌЃЌЮЊN2H4ЃЌдкГЃЮТГЃбЙЯТ0.25 molИУвКЬЌЮяжЪдкзуСПЕФбѕЦјжаЭъШЋШМЩеЩњГЩЕЊЦјКЭвКЬЌЫЎЃЌЭЌЪБЗХГіQkJЕФШШСПЁЃИУЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊN2H4(l)ЃЋO2(g) = N2(g)ЃЋ2H2O(l) H=" ЁЊ4Q" kJЁЄmolЃ1ЁЃ


 бЇСЗПьГЕЕРПкЫуаФЫуЫйЫуЬьЬьСЗЯЕСаД№АИ
бЇСЗПьГЕЕРПкЫуаФЫуЫйЫуЬьЬьСЗЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПAКЭBдквЛЖЈЬѕМўЯТПЩКЯГЩЗМЯузхЛЏКЯЮяEЃЌGдкБъзМзДПіЯТЪЧЦјЬхЃЌЧвдкДЫзДПіЯТЕФУмЖШЮЊ1.25g/LЁЃИїЮяжЪМфЯрЛЅзЊЛЏЙиЯЕШчЯТЫљЪОЃК
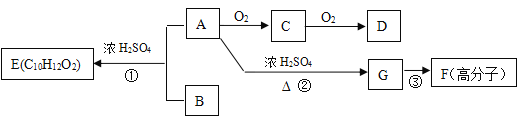
ЃЈ1ЃЉDжаЕФЙйФмЭХУћГЦЪЧ ЃЌFЕФНсЙЙМђЪНЮЊ ЁЃ
ЃЈ2ЃЉжИГіЗДгІРраЭЃКЂк ЁЃ
ЃЈ3ЃЉаДГіТњзуЯТСаЬѕМўЕФBЕФЭЌЗжвьЙЙЬхЃК ЁЃ
ЂйгіFeCl3ШмвКЯдзЯЩЋ ЂкФмЗЂЩњвјОЕЗДгІ ЂлБНЛЗЩЯжЛгаСНИіШЁДњЛљ
ЃЈ4ЃЉаДГіЛЏбЇЗНГЬЪНЃКAЁњG ЃЛ
CгыаТжЦЕФЧтбѕЛЏЭаќзЧвКЗДгІЃК ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ12ЗжЃЉвдЙшдхЭСЮЊдиЬхЕФЮхбѕЛЏЖўЗАЃЈV2O5ЃЉЪЧНгДЅЗЈЩњГЩСђЫсЕФДпЛЏМСЁЃДгЗЯЗАДпЛЏМСжаЛиЪеV2O5МШБмУтЮлШОЛЗОГгжгаРћгкзЪдДзлКЯРћгУЁЃЗЯЗАДпЛЏМСЕФжївЊГЩЗжЮЊЃК
ЮяжЪ | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
жЪСПЗжЪ§/% | 2.2-2.9 | 2.8-3.1 | 22-28 | 60-65 | 1-2 | <1 |
вдЯТЪЧвЛжжЗЯЗАДпЛЏМСЛиЪеЙЄвеТЗЯпЃК
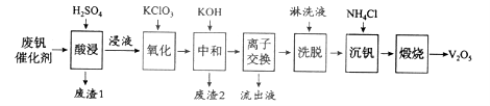
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЁАЫсНўЁБЪБV2O5зЊЛЏЮЊVO2+ЃЌЗДгІЕФРызгЗНГЬЪНЮЊ___________ЃЌЭЌЪБV2O4зЊГЩVO2+ЁЃЁАЗЯдќ1ЁБЕФжївЊГЩЗжЪЧ__________________ЁЃ
ЃЈ2ЃЉЁАбѕЛЏЁБжагћЪЙ3 molЕФVO2+БфЮЊVO2+ЃЌдђашвЊбѕЛЏМСKClO3жСЩйЮЊ______molЁЃ
ЃЈ3ЃЉЁАжаКЭЁБзїгУжЎвЛЪЧЪЙЗАвдV4O124аЮЪНДцдкгкШмвКжаЁЃЁАЗЯдќ2ЁБжаКЌга_______ЁЃ
ЃЈ4ЃЉЁАРызгНЛЛЛЁБКЭЁАЯДЭбЁБПЩМђЕЅБэЪОЮЊЃК4ROH+ V4O124![]() R4V4O12+4OHЃЈROHЮЊЧПМюадвѕРызгНЛЛЛЪїжЌЃЉЁЃЮЊСЫЬсИпЯДЭбаЇТЪЃЌСмЯДвКгІИУГЪ_____адЃЈЬюЁАЫсЁБЁЂЁАМюЁБЛђЁАжаЁБЃЉЁЃ
R4V4O12+4OHЃЈROHЮЊЧПМюадвѕРызгНЛЛЛЪїжЌЃЉЁЃЮЊСЫЬсИпЯДЭбаЇТЪЃЌСмЯДвКгІИУГЪ_____адЃЈЬюЁАЫсЁБЁЂЁАМюЁБЛђЁАжаЁБЃЉЁЃ
ЃЈ5ЃЉЁАГСЗАЁБЕУЕНЦЋЗАЫсяЇЃЈNH4VO3ЃЉГСЕэЃЌаДГіЁАьбЩеЁБжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН____________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПСзгаШ§жжЭЌЫивьаЮЬхЃЌЗжБ№ЮЊАзСзЃЈP4ЃЉЁЂКьСзКЭКкСзЁЃ
ЃЈ1ЃЉАзСзГЃЮТЮЊАзЩЋЛђЕЛЦЩЋЙЬЬхЃЌдк40ЁцзѓгвздШМЃЌЪЕбщЪвБЃДцЩйСПАзСзЕФЗНЗЈЪЧ__________ЃЛ
ЃЈ2ЃЉАзСз![]() КкСзЃЌКкСзБШАзСзЮШЖЈЁЃНсЙЙгыЪЏФЋЯрЫЦЃЌЯТСаа№Ъіе§ШЗЕФЪЧ______Ѓп
КкСзЃЌКкСзБШАзСзЮШЖЈЁЃНсЙЙгыЪЏФЋЯрЫЦЃЌЯТСаа№Ъіе§ШЗЕФЪЧ______Ѓп
AЃЎКкСзгыАзСзЛЅЮЊЭЌЗжвьЙЙЬх BЃЎКкСзФмЕМЕч
CЃЎАзСззЊЛЏЮЊКкСзЮЊбѕЛЏЛЙдЗДгІ DЃЎАзСззЊЛЏЮЊКкСзЮЊЗХШШЗДгІ
ЃЈ3ЃЉКьСздкТШЦјжаШМЩеЩњГЩСНжжТШЛЏЮяЃЌЦфжавЛжжТШЛЏЮяЗжзгЪЧУПИідзгзюЭтВуЖМТњзу8ИіЕчзгЕФНсЙЙЃЌдђИУТШЛЏЮяЕФПеМфЙЙаЭгыЯТСа_______ЗжзгзюЯрЫЦЃЈЬюзжФИЃЉ
AЃЎH2O BЃЎCCl4 CЃЎNH3 DЃЎCS2
ЃЈ4ЃЉМКжЊАзСзЁЂКьСзШМЩеЕФШШЛЏбЇЗНГЬЪНЗжБ№ЮЊ
Ђй P4(sЃЌАзСз)+5O2(gЃЉ=P4O10(s) ЁїH=-2986kJ/mol
Ђк P(sЃЌКьСз)ЃЋ![]() O2(gЃЉ=
O2(gЃЉ=![]() P4O10(s) ЁїH=-739kJ/mol
P4O10(s) ЁїH=-739kJ/mol
аДГіКьСззЊЛЏЮЊАзСзЕФШШЛЏбЇЗНГЬЪНЃК________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏКЯЮяMНаМйУлЛЗОњМзЫиЃЈШчгвЭМЃЉЃЌ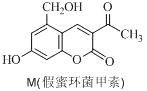 ЫќЪЧЯуЖЙЫиРрЬьШЛЛЏКЯЮяЁЃЖдMаджЪа№Ъіе§ШЗЕФЪЧ
ЫќЪЧЯуЖЙЫиРрЬьШЛЛЏКЯЮяЁЃЖдMаджЪа№Ъіе§ШЗЕФЪЧ
A. MФмгыFeCl3ЗЂЩњЗДгІЃЌВЛФмгыCH3COOHЗЂЩњЗДгІ
B. MгыBr2жЛФмЗЂЩњШЁДњЗДгІЃЌВЛФмЗЂЩњМгГЩЗДгІ
C. 1molMзюЖрПЩЯћАЂКФ3mol NaOH
D. 1molMдкДпЛЏМСзїгУЯТзюЖрФмгы4molH2ЗЂЩњМгГЩЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП ClO2ЪЧвЛжжЩБОњЯћЖОаЇТЪИпЁЂЖўДЮЮлШОаЁЕФЫЎДІРэМСЁЃЪЕбщЪвжаПЩЭЈЙ§вдЯТЗДгІжЦЕУClO2ЃК2KClO3+H2C2O4+H2SO4 ![]() 2ClO2Ёќ+K2SO4+2CO2Ёќ+2H2O ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
2ClO2Ёќ+K2SO4+2CO2Ёќ+2H2O ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
AЃЎCO2ЪЧбѕЛЏВњЮя
BЃЎH2C2O4дкЗДгІжаБЛбѕЛЏ
CЃЎ1mol KClO3ВЮМгЗДгІЃЌзЊвЦЕФЕчзгЮЊ1mol
DЃЎH2C2O4ЕФбѕЛЏадЧПгкClO2ЕФбѕЛЏад
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉЗДгІAЃЋ3B ![]() 2CЃЋ2DдкЫФжжВЛЭЌЧщПіЯТЕФЗДгІЫйТЪЗжБ№ЮЊЃК
2CЃЋ2DдкЫФжжВЛЭЌЧщПіЯТЕФЗДгІЫйТЪЗжБ№ЮЊЃК
Ђйv(A)ЃН0.15 molЁЄLЃ1ЁЄsЃ1ЃЛ
Ђкv(B)ЃН0.6 molЁЄLЃ1ЁЄsЃ1ЃЛ
Ђлv(C)ЃН0.4 molЁЄLЃ1ЁЄsЃ1ЃЛ
Ђмv(D)ЃН0.45 molЁЄLЃ1ЁЄsЃ1ЁЃ
ИУЗДгІНјааЕФПьТ§ЫГађЮЊ________________ЁЃ
ЃЈ2ЃЉдкУмБеШнЦїжаНјааПЩФцЗДгІЃЌAгыBЗДгІЩњГЩCЃЌЦфЗДгІЫйТЪЗжБ№ЮЊЃКv1ЁЂv2ЁЂv3(molЁЄLЃ1ЁЄsЃ1)ЃЌЧвv1ЁЂv2ЁЂv3жЎМфгаШчЯТЙиЯЕЃКv2ЃН3v1ЃЌv3ЃН2v1ЃЌдђДЫЗДгІЕФЛЏбЇЗНГЬЪНБэЪОЮЊ_________________ЁЃ
ЃЈ3ЃЉЯТСаИїЯюПЩвджЄУї2HI(g) ![]() H2(g)ЃЋI2(g)вбОДяЕНЦНКтзДЬЌЕФЪЧ________ЁЃ
H2(g)ЃЋI2(g)вбОДяЕНЦНКтзДЬЌЕФЪЧ________ЁЃ
ЂйЕЅЮЛЪБМфФкЩњГЩn mol I2ЕФЭЌЪБЩњГЩn mol HIЃЛ
ЂквЛИіHЁЊHМќЖЯСбЕФЭЌЪБгаСНИіHЁЊIМќЖЯСбЃЛ
ЂлАйЗжзщГЩІи(HI)ЃНІи(H2)ЪБЃЛ
ЂмЗДгІЫйТЪv(H2)ЃНv(I2)ЃНv(HI)/2ЪБЃЛ
Ђнc(H2):c(I2) :c(HI)ЃН1:1:2ЪБЃЛ
ЂоЮТЖШКЭЬхЛ§вЛЖЈЃЌШнЦїФкбЙЧПВЛдйБфЛЏЪБЃЛ
ЂпЮТЖШКЭбЙЧПвЛЖЈЃЌЛьКЯЦјЬхЕФУмЖШВЛдйБфЛЏЪБЃЛ
ЂрЮТЖШКЭЬхЛ§вЛЖЈЃЌЛьКЯЦјЬхЕФбеЩЋВЛдйБфЛЏЪБЁЃ
ЃЈ4ЃЉвбжЊЗДгІ2HI(g) = H2(g)ЃЋI2(g) ІЄHЃН11 kJЁЄmolЃ1,1 mol H2(g)ЁЂ1 mol I2(g)ЗжзгжаЛЏбЇМќЖЯСбЪБЗжБ№ашвЊЮќЪе436 kJЁЂ151 kJЕФФмСПЃЌдђ1 mol HI(g)ЗжзгжаЛЏбЇМќЖЯСбЪБашЮќЪеЕФФмСПЮЊ______kJЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПКЃЫЎПЊЗЂРћгУЕФВПЗжЙ§ГЬШчЭМЫљЪОЁЃ
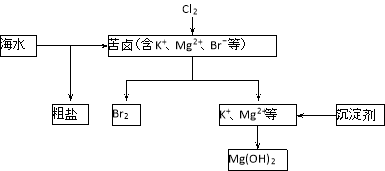
ЃЈ1ЃЉЯђПрТБжаЭЈШыCl2ЪЧЮЊСЫЬсШЁфхЃЌЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ____ЁЃ
ЃЈ2ЃЉИЛМЏфхвЛАуЯШгУПеЦјКЭЫЎеєЦјДЕГіЕЅжЪфхЃЌдйгУSO2ЕФЫЎШмвКНЋЦфЛЙдЮќЪеЃЌЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ____ЁЃвВПЩгУДПМюЮќЪефхЃЌжївЊЗДгІЪЧBr2ЃЋNa2CO3ЃЋH2OЁњNaBrЃЋNaBrO3ЃЋNaHCO3ЃЈЮДХфЦНЃЉЃЌЮќЪе1 mol Br2ЪБЃЌзЊвЦЕФЕчзгЮЊ____molЁЃ
ЃЈ3ЃЉЯТСагаЙиКЃЫЎзлКЯРћгУЕФЫЕЗЈДэЮѓЕФЪЧ____ЁЃ
AЃЎДжбЮПЩВЩгУГ§дгКЭжиНсОЇЕШЙ§ГЬЬсДП
BЃЎЕчНтБЅКЭЪГбЮЫЎПЩжЦЕУН№ЪєФЦ
CЃЎЙЄвЕЩњВњГЃбЁгУNaOHзїЮЊГСЕэМС
DЃЎКЃЫЎЬсУОЩцМАЕНИДЗжНтЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
AЃЎБНЗгЕФЫзГЦЃКЪЏЬПЫс
BЃЎCH3COCH3ЗжзгжаЕФЙйФмЭХУћГЦЃКУбМќ
CЃЎЦЯЬбЬЧЕФЪЕбщЪНЃКCH2O
DЃЎввШВЕФНсЙЙМђЪНЃКCHЁдCH
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com