
| A£® | š¤ĶĮ | B£® | “æ¼ī”¢ŹÆ»ŅŹÆ”¢ŹÆӢɰ | ||
| C£® | š¤ĶĮ”¢ŹÆ»ŅŹÆ | D£® | ¶žŃõ»Æ¹č”¢¹čĖįøĘ”¢¹čĖįĀĮ |
·ÖĪö š¤ĶĮŹĒÖĘ×÷שĶßŗĶĢՓɵÄÖ÷ŅŖŌĮĻ£¬Ė®»š¼Č¼Ć¶ųĶĮŗĻ£®”ĖłŹöµÄ”°ĢÕ³ÉŃÅĘ÷”±µÄÖ÷ŅŖŌĮĻŹĒš¤ĶĮ£®
½ā“š ½ā£ŗĢՓɵē«Ķ³øÅÄīŹĒÖøĖłÓŠŅŌš¤ĶĮµČĪŽ»ś·Ē½šŹōæóĪļĪŖŌ²ÄĮĻ£¬¾¹żøßĪĀÉÕÖʶų³ÉµÄ²śĘ·£¬ĢāøÉÖŠĢÕ³ÉŃÅĘ÷£¬Ė®»š¼Č¼Ć¶ųĶĮŗĻĪŖĢÕĘ÷µÄÉś²ś¹¤ŅÕ£¬ĖłŅŌĖłŹöµÄ”°ĢÕ³ÉŃÅĘ÷”±µÄÖ÷ŅŖŌĮĻŹĒš¤ĶĮ£¬
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖĢՓɵÄÓŠ¹ŲÖŖŹ¶£¬ÕĘĪÕš¤ĶĮŹĒÖĘ×÷שĶßŗĶĢՓɵÄÖ÷ŅŖŌĮĻŹĒ½ā“š¹Ų¼ü£¬ĢāÄæ½Ļ¼ņµ„£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
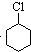 £ØŅ»ĀČ»·¼ŗĶ飩$”ś_{¢Ś}^{NaOH£¬ŅŅ“¼£¬”÷}$
£ØŅ»ĀČ»·¼ŗĶ飩$”ś_{¢Ś}^{NaOH£¬ŅŅ“¼£¬”÷}$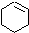 $”ś_{¢Ū}^{Br_{2}µÄCClČÜŅŗ}$
$”ś_{¢Ū}^{Br_{2}µÄCClČÜŅŗ}$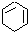 $\stackrel{¢Ü}{”ś}$
$\stackrel{¢Ü}{”ś}$ £¬Ćū³ĘŹĒ»·¼ŗĶé
£¬Ćū³ĘŹĒ»·¼ŗĶé £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
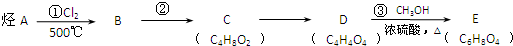
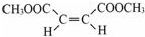 £»ŌŚĘäHNMRĘ×ÖŠ£¬ÓŠ2Öַ壬Ęä·åĆ껿±ČĪŖ1£ŗ3£®EÄÜ·¢Éś¾ŪŗĻ·“Ó¦£¬Š“³öĘä»Æѧ·½³ĢŹ½
£»ŌŚĘäHNMRĘ×ÖŠ£¬ÓŠ2Öַ壬Ęä·åĆ껿±ČĪŖ1£ŗ3£®EÄÜ·¢Éś¾ŪŗĻ·“Ó¦£¬Š“³öĘä»Æѧ·½³ĢŹ½
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
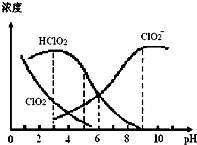 ŃĒĀČĖįÄĘ£ØNaClO2£©ŌŚČÜŅŗÖŠæÉÉś³ÉClO2”¢HClO2”¢ClO2-”¢Cl-µČ£¬ĘäÖŠHClO2ŗĶClO2¶¼¾ßÓŠĘÆ°××÷ÓĆ£¬µ«ClO2ŹĒÓŠ¶¾ĘųĢ壮ijĪĀ¶ČĻĀ£¬²æ·Öŗ¬ĀČ×é·Öŗ¬ĮæĖępH±ä»ÆĒéæöČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ŃĒĀČĖįÄĘ£ØNaClO2£©ŌŚČÜŅŗÖŠæÉÉś³ÉClO2”¢HClO2”¢ClO2-”¢Cl-µČ£¬ĘäÖŠHClO2ŗĶClO2¶¼¾ßÓŠĘÆ°××÷ÓĆ£¬µ«ClO2ŹĒÓŠ¶¾ĘųĢ壮ijĪĀ¶ČĻĀ£¬²æ·Öŗ¬ĀČ×é·Öŗ¬ĮæĖępH±ä»ÆĒéæöČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | Ź¹ÓĆøĆĘÆ°×¼ĮµÄŹŹŅĖpHŌ¼ĪŖ5.0 | |
| B£® | øĆĪĀ¶ČĻĀNaClO2ČÜŅŗÖŠ£ŗc£Ø Na+£©£¾c£ØClO2-£©£¾c£ØOH-£©£¾c£ØH+£© | |
| C£® | ²»Ķ¬pHµÄNaClO2ČÜŅŗÖŠ“ęŌŚĻĀĮŠ¹ŲĻµ£ŗc £Ø Na+£©=c£ØClO2-£©+c£ØHClO2£©+c£ØClO2£© | |
| D£® | øĆĪĀ¶ČĻĀHClO2µÄµēĄėĘ½ŗā³£ŹżµÄŹżÖµ£ŗKa”Ö1.0”Į10-6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µČĪļÖŹµÄĮæµÄO2ŗĶCO2Ėłŗ¬ŃõŌ×ÓŹż¾łĪŖ2NA | |
| B£® | ±ź×¼×“æöĻĀ£¬2.24 LŅ»ĀČ¼×ĶéÖŠŗ¬ÓŠĒāŌ×ÓŹżÄæĪŖ0.3NA | |
| C£® | ŌŚ·“Ó¦KIO3+6HI=KI+3I2+3H2OÖŠ£¬ĆæÉś³É3mol I2×ŖŅʵĵē×ÓŹżĪŖ6NA | |
| D£® | 6.8 gČŪČŚµÄKHSO4ÖŠŗ¬ÓŠ0.1 NAøöŃōĄė×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹµŃéŹŅÖĘĒāĘų£¬ĪŖĮĖ¼Óæģ·“Ó¦ĖŁĀŹ£¬æɽ«Ļ”ĮņĖįøijÉÅØĮņĖį | |
| B£® | ĪŖ“¦Ąķ¹ųĀÆĖ®¹øÖŠµÄCaSO4£¬æÉĻČÓƱ„ŗĶNa2CO3ČÜŅŗ½žÅŻ£¬ŌŁ¼ÓČėŃĪĖįČܽā | |
| C£® | N2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H£¼0£¬ĘäĖūĢõ¼ž²»±äŹ±ÉżøßĪĀ¶Č£¬ĒāĘų×Ŗ»ÆĀŹŌö“ó | |
| D£® | ·“Ó¦4Fe£ØOH£©2£Øs£©+O2£Øg£©+2H2O£Øl£©=4Fe£ØOH£©3£Øs£©µÄ”÷H£¾0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
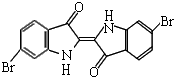 Ģ©ŃÅ×ĻŹĒ¹Å“śµŲÖŠŗ£ŃŲ°¶³ö²śµÄŅ»ÖÖ¹óÖŲČ¾ĮĻ£¬ĻÖÖŖĘä½į¹¹ĪŖČēĶ¼ĖłŹ¾µÄŗ¬äåÓŠ»ś»ÆŗĻĪļ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
Ģ©ŃÅ×ĻŹĒ¹Å“śµŲÖŠŗ£ŃŲ°¶³ö²śµÄŅ»ÖÖ¹óÖŲČ¾ĮĻ£¬ĻÖÖŖĘä½į¹¹ĪŖČēĶ¼ĖłŹ¾µÄŗ¬äåÓŠ»ś»ÆŗĻĪļ£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | Ģ©ŃÅ×Ļ·Ö×ӵķÖ×ÓŹ½ĪŖC16H8N2Br2O2 | |
| B£® | 1molĢ©ŃÅ×ĻÓėH2¼Ó³É×ī¶ąŠč9molH2 | |
| C£® | Ģ©ŃÅ×ĻŹōÓŚĢžµÄŃÜÉśĪļ | |
| D£® | ¼ģŃéĢ©ŃÅ×ĻÖŠäåŌŖĖŲæÉÖ±½Ó¼ÓČėĻõĖįŅųČÜŅŗ£¬¹Ū²ģŹĒ·ńÓŠĒ³»ĘÉ«³ĮµķÉś³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2ÄÜŹ¹äåĖ®ĶŹÉ«£¬ĢåĻÖĘäĘư׊Ō | |
| B£® | NOx”¢CO2”¢PM 2.5æÅĮ£¶¼»įµ¼ÖĀĖįÓź | |
| C£® | ÄĘ¼ŲŗĻ½šæÉÓĆÓŚæģÖŠ×Ó·“Ó¦¶ŃµÄČČ½»»»¼Į | |
| D£® | µČÖŹĮæµÄNaHCO3°“a”¢bĮ½ÖÖĶ¾¾¶ĶźČ«×Ŗ»Æ£¬Ķ¾¾¶a±ČĶ¾¾¶bĻūŗÄøü¶ąµÄŃĪĖį Ķ¾¾¶a£ŗNaHCO3 $\stackrel{”÷}{”ś}$Na2CO3 $\stackrel{ŃĪĖį}{”ś}$CO2£»Ķ¾¾¶b£ŗNaHCO3$\stackrel{ŃĪĖį}{”ś}$CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
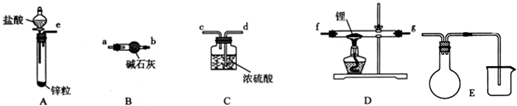
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com