
【题目】下列实验的相关描述正确的是( )
A.快速分离氢氧化铁胶状沉淀和氯化钠溶液可用抽滤法
B.常温下,苯酚与水形成的浊液静置后会分层,上层为溶有水的苯酚溶液
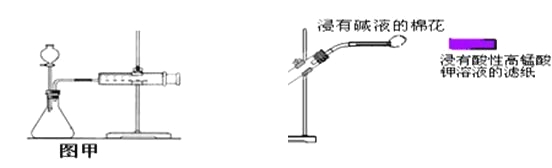
C.甲装置可用于某些化学反应速率的测定。该装置气密性的检查如下:仪器组装好后,关闭分液漏斗活塞,将针筒活塞向外拉一段距离后松手,观察针筒是否能回到原来刻度处
D.用氢氧化钠滴定醋酸实验,酸式滴定管没有润洗就直接使用则所得待测液浓度偏高
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下。
[实验目的] 测量锌和稀硫酸反应的速率。
[实验用品] 锥形瓶、双孔塞、分液漏斗、直角导管、50 mL注射器、铁架台、秒表、锌粒、1 mol·L-1的H2SO4、4 mol·L-1的H2SO4。
[实验步骤]
(1)甲同学取一套如图装置,加入40 mL 1 mol·L-1的H2SO4,测量收集10 mL H2所需的时间。

(2)乙同学取另一套同样的装置,加入40 mL 4 mol·L-1的H2SO4,测量收集10 mL H2所需的时间。
回答下列问题:
(1)Zn与稀H2SO4反应的离子方程式为________。
(2)收集10 mL H2所需时间:甲________(填“大于”“小于”或“等于”)乙。反应速率:甲________(填“大于”“小于”或“等于”)乙。
(3)下列说法正确的是________(填字母)。
A 本实验中甲、乙两同学所用锌粒的表面积要相同
B 装置气密性要好
C 40 mL的H2SO4要迅速加入
D 测量气体体积还可以用排水法
E 若用98%的浓H2SO4,则反应最快
(4)测定Zn和稀H2SO4反应的速率还可用的方法有:①___________; ②_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,向某恒容密闭容器中加入1.6 molL-1的W后会发生如下反应:2W(g)=M(g) △H =a kJ mol-1。其中M的物质的量浓度随时间的变化如图所示:
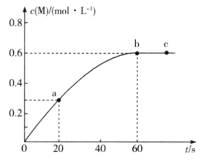
下列说法错误的是
A.从反应开始到刚达到平衡时间段内,υ(W) =0.02 molL-1s-1
B.a、b两时刻生成W的速率:υ(a)<υ(b)
C.用W浓度变化值表示的ab、bc两个时段内的反应速率:υ(ab)>υ(bc) =0
D.其他条件相同,起始时将0.2 mol L-1氦气与W混合,则反应达到平衡所需时间少于60 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氨气的说法正确的是
A.氨既能用浓硫酸干燥也能用无水CaCl2干燥
B.NH3是电解质,所以氨水能导电
C.NH3可以使干燥的红色石蕊试纸变蓝
D.用水吸收NH3用如图装置可防止倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定温度下的恒容密闭容器中,可逆反应达到平衡状态时,一些宏观物理量恒定不变:a.各物质的浓度不变,b.平衡混合物中各组分的物质的量分数或质量分数不变,c.容器内气体压强不变,d.容器内气体密度不变,e.容器内气体颜色不变。
①能说明反应N2(g)+3H2(g) ![]() 2NH3(g)达到平衡状态的有__;
2NH3(g)达到平衡状态的有__;
②能说明反应H2(g)+I2(g) ![]() 2HI(g)达到平衡状态的有__;
2HI(g)达到平衡状态的有__;
(2)为了研究碳酸钙与盐酸反应的反应速率,某同学通过如图实验装置测定反应中生成的CO2气体体积,并绘制出如图所示的曲线。请分析讨论以下问题。
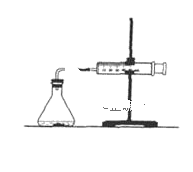
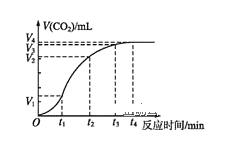
①化学反应速率最快的时间段是___(填选项),影响此时间段反应速率的主要因素是___;
A.O~t1 B.t1~t2 C.t2~t3 D.t3~t4
②为了减缓上述反应速率,欲向盐酸中加入下列物质,你认为可行的有___;
A.蒸馏水 B.NaCl固体 C.NaCl溶液 D.通入HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法不正确的是
A.5.5g超重水(T2O)中含有的中子数目为3NA
B.常温常压下,44gCO2与足量过氧化钠反应转移电子的数目为NA
C.常温常压下,42gC2H4和C4H8混合气体中含有氢原子的数目为6NA
D.0.1L0.5mol·L-1CH3COOH溶液中含有H+数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中可进行反应A+B![]() C+D,其中A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的图线。(0~t1、t1~t2、t2~t3各时间段相同)下列说法不正确的是
C+D,其中A、B在一定条件下反应并测定反应中生成物C的浓度随反应时间的变化情况,绘制出如图所示的图线。(0~t1、t1~t2、t2~t3各时间段相同)下列说法不正确的是

A. 该反应是吸热反应
B. 反应速率最大的时间段是在t1~t2
C. 四个时间段内生成C的量最多的是t1~t2
D. 反应速率后来减慢主要是受反应物浓度变化的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
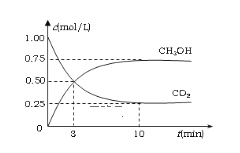
(1)在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+ H2O(g) △H =-49.0kJ/mol 。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+ H2O(g) △H =-49.0kJ/mol 。测得CO2和CH3OH(g)的浓度随时间变化如图所示。
①氢气的转化率=__________________;
②该反应的平衡常数为___________(保留小数点后2位);
③下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是___________。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去 D.再充入1mol CO2和3mol H2
④当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2。则c1______c2的关系(填>、<、=)。
(2)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______。
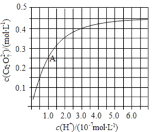
(3)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol·L1的Na2CrO4溶液中c(Cr2O72) 随c(H+)的变化如图所示。①离子方程式表示Na2CrO4溶液中的转化反应_________________。②由图可知,溶液酸性增大,CrO42的平衡转化率____(填“增大“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1 mol ClOx-(x=0,1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法错误的是
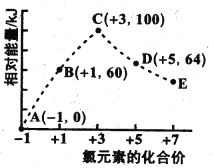
A. 上述离子中结合H能力最强的是E
B. 上述离子中最稳定的是A
C. C→B+D反应的热化学方程式为2ClO2-(aq)=ClO3-(ag)+ClO-(aq) △H=-76kJ·mol-1
D. B→A+D的反应物的键能之和小于生成物的键能之和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com