
| |||||||||||||||||||||||||

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ������2011�����12���������м�⻯ѧ����B�� ���ͣ�022
�״�(
CH3OH)��һ����Ҫ�Ļ���ԭ�ϣ��㷺Ӧ���ڻ���������Ҳ����ֱ������ȼ�ϣ���֪CH3OH(1)��O2(g)��CO(g)��2H2O(g)����Ha����443.64 kJ��mol��1
2CO(g)��O2(g)��2CO2(g)����Hb����566.0 kJ��mol��1
(
1)��д��CH3OH(1)����������ȫȼ������CO2��H2O(g)���Ȼ�ѧ����ʽ��________
(
2)�״���Ϊȼ�ϣ������ŵ���ȼ��ʱ�ŷŵ���Ⱦ���٣��Ӷ������ܻ�����Դ���ź�����ЧӦ�����⣬���ܸ��ƴ���������������(1)�е��Ȼ�ѧ����ʽ���㣬��ȫȼ��20 g�״������ɶ�����̼��ˮ����ʱ���ų�������Ϊ________kJ�����ɵ�CO2�����״���������________L��(
3)������Ա�½�������һ���ɼ״���������ǿ�����������Һ�������ֻ���أ���ʹ�ֻ�����ʹ��һ���²ų�һ�ε磬�ݴ˻ش��������⣺�״���
________����Ӧ���缫��ӦʽΪ________��(
4)���õ�ؿ�ʵ�ֵ�����ѧ��ת����ijͬѧ�����һ�ֵ�ⷨ��ȡFe(OH)2��ʵ��װ��(����ͼ��ʾ)��ͨ�����Һ�в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ��
����˵������ȷ����
________(�����)A��
��Դ�е�aһ��Ϊ������bһ��Ϊ����B��
������NaCl��Һ��Ϊ���ҺC��A
��B���˶������������缫D��
���������ķ�Ӧ�ǣ�2H+��2e����H2����������
Fe(OH)2������¶�ڿ����У�����ɫ�仯��________����Ӧ�Ļ�ѧ����ʽΪ________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��������ʡģ���� ���ͣ������
 CH3OH(g) ��H=
CH3OH(g) ��H=

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ͬ���� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Դ��������ᷢչ���������ʻ�������Դ����Ϣ������һ�����ִ�����������֧�����״�(CH3OH)��һ����Ҫ�Ļ���ԭ�ϣ��㷺Ӧ���ڻ���������Ҳ����ֱ������ȼ�ϣ�������������������β���Դ�������Ⱦ��
����д���״��ĵ���ʽ_ __����״������ʵ�����ͬ��ij�л����ȫȼ��ʱ���ĵ���������Ҳ��״���ͬ��д������������������һ�л���Ļ�ѧʽ__ __��
����֪CH30H(1)+O2 (g)��CO(g)+2H2O(g) ![]()
2CO(g)+O2 (g)��2CO2 (g) ![]()
(1)��д��CH3OH(1)��ȫȼ��[����H2O(g)]���Ȼ�ѧ����ʽ��
(2)���˽��飬Ͷ���о���CO2��H2O(g)����ȡCH3OH(1)������ɹ������ܻ�����Դ���ţ����ܽ������ЧӦ�����⡣���������֤���ý����Ƿ����?
��(1)�Լ״���Һ������Ϊ������Ӧ�������ȼ�ϵ���Ѿ���������ṹ��ͼ��ʾ(�״����������H+����ͨ�����ӽ���Ĥ������һ��)����д���״��ڵ缫�Ϸ�Ӧ�ķ���ʽ��________, ����32g�״�����ȫ����ʱ��ת�Ƶ���____mo1��
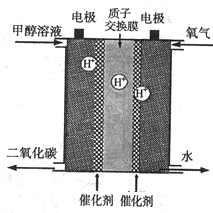
(2)ijͬѧ�Լ״�ȼ�ϵ��Ϊ��Դ������ʯīΪ�缫���CuSO4��Һ�������Դ���������ĵ��ص缫�ϵĵ缫��ӦʽΪ____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �״�(CH3OH)��һ����Ҫ�Ļ���ԭ�ϣ��㷺Ӧ���ڻ���������Ҳ����ֱ������ȼ�ϡ���֪CH3OH(l)O2(g)=CO(g)+2H2O(g) ��Ha=-443.64KJ?mol-1 2CO(g)+O2(g)=2CO2(g)
�״�(CH3OH)��һ����Ҫ�Ļ���ԭ�ϣ��㷺Ӧ���ڻ���������Ҳ����ֱ������ȼ�ϡ���֪CH3OH(l)O2(g)=CO(g)+2H2O(g) ��Ha=-443.64KJ?mol-1 2CO(g)+O2(g)=2CO2(g)
��Hb=-566.0KJ?mol-1
(1)��д��CH3OH(l)����������ȫȼ������CO2��H2O(��)���Ȼ�ѧ����ʽ�� ____________________________________________________________________________________________________________
(2)������Ϊ����һ�������£���ȫ��ʵ����CO2��H2O(��)����ȡCH3OH(l)�ķ�Ӧ���Ӷ��ܻ�����Դ���ź�����ЧӦ�����⡣��ͨ������˵�������ַ�Ӧ�Ƿ���п�����?
(3)������Ա�½�������һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ���ʹ�ֻ�����ʹ��һ���²ų�һ�ε磬�ݴ˻ش��������⣺
�״���__________����Ӧ���缫��ӦʽΪ____________________________________________
(4)���õ�ؿ�ʵ�ֵ�����ѧ��ת����ijͬѧ�����һ�ֵ�ⷨ��ȡFe(OH)2��ʵ��װ�ã�ͨ�����Һ�в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ������˵������ȷ����_____(�����)
A�� ��Դ�е�aһ��Ϊ������bһ��Ϊ����
B�� ������NaCl��Ϊ���Һ
C�� A��B���˶������������缫
D�� ���������ķ�Ӧ�ǣ�2H++2e-��H2��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com