
【题目】将7.2gCO和H2的混合气体与足量O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加 ( )
A. 2.1g B. 3.6g C. 7.2g D. 无法确定
【答案】C
【解析】2CO+O2![]() 2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;2H2+O2
2CO2,一氧化碳与二氧化碳物质的量相等,Na2O2与CO2反应2CO2+2Na2O2=2Na2CO3+O2,质量增重△m=2Na2CO3-2Na2O2=2CO,可知反应后固体质量增加量为CO的质量;2H2+O2![]() 2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2=4NaOH+O2↑,质量增重△m=2H2O-O2=2H2,可知,反应后固体增加的质量为氢气质量.所以将7.2gCO和H2的混合气体在足量氧气中充分燃烧后的产物立即通入盛有足量Na2O2的反应管,固体质量增重为7.2gCO和H2的混合气体的质量;答案选C。
2H2O,生成的水与氢气物质的量相等,Na2O2与H2O反应2H2O+2Na2O2=4NaOH+O2↑,质量增重△m=2H2O-O2=2H2,可知,反应后固体增加的质量为氢气质量.所以将7.2gCO和H2的混合气体在足量氧气中充分燃烧后的产物立即通入盛有足量Na2O2的反应管,固体质量增重为7.2gCO和H2的混合气体的质量;答案选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】同一周期三种非金属元素X、Y、Z,其最高价氧化物的水化物的酸性由强到弱的顺序是:HXO4>H2YO4>H3ZO4。下列说法正确的是( )
A.元素的非金属性:X<Y<Z
B.气态氢化物的稳定性:HX>H2Y>ZH3
C.阴离子的还原性:X->Y2->Z3-
D.X、Y、Z依次位于ⅤA族、ⅥA族、ⅦA族。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两个小组利用酸性KMnO4与H2C2O4溶液反应,设计实验探究影响反应速率的因素(2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2+8H2O) 甲组:利用如图装置,通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小.(实验中所用KMnO4溶液均已加入H2SO4)
序号 | A溶液 | B溶液 |
① | 2ml 0.2mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液 |
② | 2ml 0.1mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液 |
③ | 2ml 0.2mol/LH2C2O4溶液 | 4ml 0.01mol/LKMnO4溶液和少量MnSO4 |
(1)该实验的目的是探究对化学反应速率的影响.
(2)分液漏斗中A溶液应该加入(填“一次性”或“逐滴滴加”)
(3)实验结束后,读数前为了使两个量气管的压强相等,避免产生压强差,影响测定结果,需要进行的操作是 . 乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率为了探究KMnO4与H2C2O4浓度对反应速率的影响,某同学在室温下完成以下实验
实验编号 | 1 | 2 | 3 | 4 |
水/ml | 10 | 5 | 0 | X |
0.5mol/L H2C2O4/ml | 5 | 10 | 10 | 5 |
0.2mol/L KMnO4/ml | 5 | 5 | 10 | 10 |
时间/s | 40 | 20 | 10 | ﹣﹣﹣ |
(4)X= A.5 B.10 C.15 D.20
4号实验中始终没有观察到溶液褪色,你认为可能的原因是 . 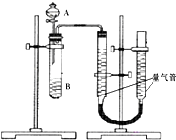
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知相同条件下,下列反应的焓变和乎衡常数分别表示为: ①2H2O(g)=O2(g)+2H2(g)△H1 K1=x
②Cl2(g)+H2(g)=2HCl(g)△H2 K2=y
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3 K3=x
则下列关系正确的是( )
A.△H3=△H1+2△H2 x=xy2
B.H3=△H1+△H2 z=x+y
C.H3=△H1+2△H2 x=x﹣y2
D.H3=△H1+△H2 z= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙酸性质的叙述中,错误的是
A. 乙酸的酸性比碳酸强,所以它可以与碳酸盐反应,产生CO2气体
B. 乙酸能与醇类物质发生酯化反应
C. 乙酸分子中含有碳氧双键,所以它能使溴水褪色
D. 乙酸在温度低于16.6 ℃时,就凝结成冰状晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请预测有机物丙烯酸(CH2=CH-COOH)的发生的反应类型可能有( )
①加成反应②水解反应③酯化反应④中和反应⑤氧化反应.
A. 只有①③B. 只有①③④C. ①②③④⑤D. 只有①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是_____.
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
沉淀固体B______;C________;沉淀D_____;溶液E________.
(3)写出①、②、③、④四个反应方程式
①_________________________;
②________________________;
③________________________;
④________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一份含有杂质MgCl2和KCl的AlCl3溶液M,某小组用下图所示过程对其进行除杂并尽可能的减少AlCl3的损失。请回答下列问题:

(1)沉淀A的化学式为__________,过程①中Al3+发生反应的离子方程式为__________________。
(2)氢氧化钠溶液_____(填“能”或“不能”)用氨水代替,原因是_____________________。
(3)溶液B中大量存在的阳离子是______________,过程②中生成沉淀C的离子方程式为_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com