
 Ⅰ、已知 KI溶液在酸性条件下能与氧气反应. 现有以下实验记录:
Ⅰ、已知 KI溶液在酸性条件下能与氧气反应. 现有以下实验记录:| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度(℃) | 30 | 40 | 50 | 60 | 70 |
| 显色时间(s) | 160 | 80 | 40 | 20 | 10 |
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
分析 Ⅰ、(1)根据氧化还原反应类型离子方程式要遵循原子守恒、电荷守恒和得失电子数目相等书写;
(2)根据表中数据分析,该实验目的是探究温度对反应速率的影响;
(3)为测定显色时间,产物中有碘单质生成,还需要的试剂是淀粉溶液,实验现象为无色溶液变蓝色;
(4)分析实验数据可得出的结论是每升高10℃,反应速率增大约2倍;
(5)若要进行酸性对反应速率的影响的探究实验,你会采取的措施是保持其他实验条件不变,采用不同浓度的硫酸溶液进行对比实验;
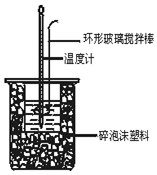
Ⅱ、根据中和热计算公式Q=cm△T中涉及的未知数据进行判断;
先根据表中测定数据计算出混合液反应前后的平均温度差,再根据Q=cm△T计算出反应放出的热量,最后计算出中和热;
反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答.
解答 解:Ⅰ、(1)碘离子被氧气氧化生成单质碘,氧气在酸性条件下还原成水,该反应的离子方程式为:4H++4I-+O2=2I2+2H2O;
故答案为:4H++4I-+O2=2I2+2H2O;
(2)根据表中数据分析,该实验目的是探究温度对反应速率的影响;
故答案为:探究温度对反应速率的影响;
(3)为测定显色时间,产物中有碘单质生成,还需要的试剂是淀粉溶液,实验现象为无色溶液变蓝色;
故答案为:淀粉溶液;无色溶液变蓝色;
(4)分析实验数据可得出的结论是每升高10℃,反应速率增大约2倍;
故答案为:每升高10℃,反应速率增大约2倍;
(5)若要进行酸性对反应速率的影响的探究实验,你会采取的措施是保持其他实验条件不变,采用不同浓度的硫酸溶液进行对比实验;
故答案为:保持其他实验条件不变,采用不同浓度的硫酸溶液进行对比实验;
Ⅱ、由Q=cm△T可知,测定中和热需要测定的数据为:A.反应前盐酸溶液的温度、C.反应前氢氧化钠溶液的温度、E.反应后混合溶液的最高温度;
第1次实验盐酸和NaOH溶液起始平均温度为20.05℃,反应后温度为:23.2℃,反应前后温度差为:3.15℃;
第2次实验盐酸和NaOH溶液起始平均温度为20.3℃,反应前后温度差为:3.1℃;
第3次实验盐酸和NaOH溶液起始平均温度为20.55℃,反应前后温度差为:3.05℃;
3次实验数据均有效,温度差平均值为3.1℃,
40mL 0.50mol/L盐酸与 40mL 0.50mol/LNaOH溶液的质量和m=80mL×1g/cm3=80g,c=4.18J/(g•℃),代入公式Q=cm△T得生成0.02mol的水放出热量Q=4.18J/(g•℃)×80g×3.1℃=1.036kJ,即生成0.02mol的水放出热量为:1.036kJ,所以生成1mol的水放出热量为1.036kJ×$\frac{1mol}{0.02mol}$=-51.8kJ/mol,即该实验测得的中和热△H=-51.8kJ/mol;
反应放出的热量和所用酸以及碱的量的多少有关,改用100mL 0.50mol/L盐酸跟100mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,生成水的量增加,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以改用100mL 0.50mol/L盐酸跟100mL 0.55mol/L NaOH溶液进行反应,测得中和热数值相等;
故答案为:ACE;-51.8kJ/mol;相等.
点评 本题题以KI溶液在酸性条件下与氧气的反应为载体,提高实验探究温度等外界条件对化学反应速率的影响规律,反应热测定与计算,注意理解中和热测定原理以及测定反应热的误差等问题,试题有利于培养学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:选择题
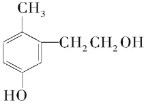
| A. | 它是苯酚的同系物 | |
| B. | 1 mol该物质能与溴水反应消耗2molBr2发生取代反应 | |
| C. | 1 mol该有机物能与足量金属钠反应生成0.5mol H2 | |
| D. | 1 mol该有机物能与2molNaOH反应 | |
| E. | 该物质在加热条件下可以与铜反应生成一种具有醛基的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气还原氧化铜当反应完成后,先停止通氢气再停止加热 | |
| B. | 将饱和FeCl3溶液加热煮沸来制备Fe(OH3胶体) | |
| C. | 工业制备HCl气体时将氢气和氯气的混合气体在光照条件下反应 | |
| D. | 浓硫酸稀释时如图操作 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4(g)+$\frac{3}{2}$O2(g)═2H2O(l)+CO(g)△H1 | B. | 2CO(g)+O2(g)═2CO2(g)△H2 | ||
| C. | S(s)+$\frac{3}{2}$O2(g)═SO3(s)△H3 | D. | C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com