
【题目】2-甲基丁烷跟氯气发生取代反应后得到一氯代物的同分异构体有( )
A. 2种 B. 3种 C. 4种 D. 5种
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】为解决大气中CO2的含量增大的问题,某科学家提出“绿色自由”构想:把工厂排出的富含CO2的废气经净化吹入碳酸钾溶液吸收,然后再把CO2从溶液中提取出来,经化学反应使废气中的CO2转变为燃料甲醇.“绿色自由”构想的部分技术流程如图1 
(1)合成塔中反应的化学方程式为;△H<0.从平衡移动原理分析,低温有利于提高原料气的平衡转化率.而实际生产中采用300℃的温度,除考虑温度对反应速率的影响外,还主要考虑了 .
(2)从合成塔分离出甲醇的原理与下列操作的原理比较相符(填字母)
A.过滤
B.分液
C.蒸馏
D.结晶
(3)在体积为2L的合成塔中,充人2mol CO2和6mol H2 , 测得CO2(g)和CH3OH(g)的浓度随时间变化如图2所示. 从反应开始到平衡,V(H2)=;能使平衡体系中 ![]() 增大的措施有 .
增大的措施有 .
(4)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4 . 巳知
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=﹣890.3kJ/mol
H2(g)+ ![]() O2(g)═H2O(l)△H2=﹣285.5kJ/mol
O2(g)═H2O(l)△H2=﹣285.5kJ/mol
写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向MgSO4和Al2(SO4)3的混合溶液中,逐滴加入NaOH溶液.下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)( )
A.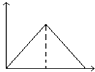
B.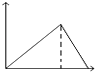
C.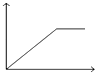
D.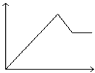
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为4种常见溶液中溶质的质量分数和物质的量浓度:
溶质 | HCl | NaOH | CH3COOH | HNO3 |
溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
物质的量浓度/mol·L1 | 11.8 | 14.3 | 10.6 | 13.8 |
这4种溶液中密度最小的是
A.HCl B.NaOH C.CH3COOH D.HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂用软锰矿(含MnO2及少量Al2O3)和闪锌矿(含ZnS及少量FeS)联合生产Zn、MnO2 , 其部分生产流程如下: 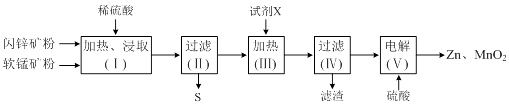
已知:过滤(Ⅱ)所得滤液是MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液.相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0molL﹣1计算)如下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Zn(OH)2 | Mn(OH)2 |
开始沉淀时的pH | 2.7 | 4.0 | 6.4 | 7.7 |
完全沉淀时的pH | 3.7 | 5.2 | 8.0 | 10.4 |
(1)加热、浸取时所加矿石均需粉碎,其目的是 .
(2)写出FeS和MnO2和稀硫酸反应的离子方程式: .
(3)试剂X的作用是调节溶液的pH以生成Fe(OH)3、Al(OH)3 . pH调节的范围是 , 试剂X可以选用(填选项字母).
A.MnCO3 B.Na2CO3 C.Zn2(OH)2CO3 D.NH3H2O
(4)电解(Ⅴ)中阳极的电极反应式为 .
(5)Zn和MnO2是制作电池的原料.某锌﹣锰碱性电池以KOH溶液为电解质溶液,其电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s).该电池的正极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,按单质、化合物、混合物的顺序排序正确的是
A.稀有气体、尿素、冰水混合物
B.乙醇、浓硫酸、胆矾
C.金刚石、铁矿石、大理石
D.水银、水蒸气、水煤气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列五组物质:A、O2和O3 B、3517Cl和3717Cl C、CH4与C7H16 D、CH3CH2CH2CH3 与 ![]()
(1)组两种物质互为同位素;
(2)组两种物质互为同素异形体;
(3)组两种物质互为同系物;
(4)组两种物质互为同分异构体.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组为探究铜与浓硫酸的反应,用右图所示的装置进行实验: 请回答下列问题:
(1)B是用来收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整. 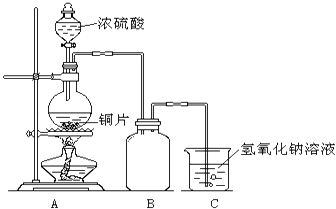
(2)实验中他们取6.4g铜片和12mL18molL﹣1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余. ①写出铜与浓硫酸反应的化学方程式: ,
实验中若有m g铜参加了反应,则有mol硫酸被(填“氧化”或“还原”),转移电子的物质的量为mol.
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是(填写字母编号).
A.硫酸钠溶液 B.氯化钡溶液 C.银粉 D.碳酸钠溶液
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?你认为的原因是
(3)为了测定剩余硫酸的物质的量浓度,该兴趣小组设计了三个实验方案: 方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次质量差即是吸收的二氧化硫.
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量.
方案三:当铜和浓硫酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生氢气的体积为V L(已换算为标准状况).
实际上,以上方案一、二均不可取,请你说出原因?
方案一;
方案二 .
方案三:写出剩余硫酸的物质的量浓度的计算式(假设反应后溶液的体积仍为12mL) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com