
下列符合“化学反应的绿色化”的是( )
A.实验室制O2:2KClO3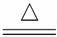 2KCl+3O2↑
2KCl+3O2↑
B.2C2H5OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
C.2M+N2P+2Q,2P+M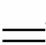 Q(M、N为原料,Q为期望产品)
Q(M、N为原料,Q为期望产品)
D.用铁屑、CuO、稀硫酸为原料制铜:CuO+H2SO4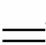 CuSO4+H2O,Fe+CuSO4
CuSO4+H2O,Fe+CuSO4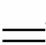 FeSO4+Cu
FeSO4+Cu
科目:高中化学 来源: 题型:
下列关于电解质的叙述正确的是( )
A.强酸、强碱及大部分盐类属于强电解质,弱酸、弱碱属于弱电解质
B.所有的离子化合物都是强电解质,所有的共价化合物都是弱电解质
C.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
D.CO2的水溶液能导电,所以CO2是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
依据氧化还原反应: 2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
(1)电极X的材料是______;电解质溶液Y是________;
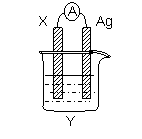 (2)银电极为电池的____极,发生的电极反应式为_______ ___;X电极上发生的电极反应为_____________________;(填反应类型)
(2)银电极为电池的____极,发生的电极反应式为_______ ___;X电极上发生的电极反应为_____________________;(填反应类型)
(3)外电路中的电子是从_______电极流向________电极。
(4)当有1.6g铜溶解时,银棒增重_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①A+B2+===A2++B ②D+2H2O===D(OH)2+H2↑ ③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-===E,B-2e-===B2+,下列说法正确的是
A.氧化性E2+>B2+>A2+>D2+
B.氧化性D2+>E2+>A2+>B2+
C.反应E+A2+===A+E2+能够进行
D.提取某废水中含有少量的A2+时可以选用D
查看答案和解析>>
科目:高中化学 来源: 题型:
仔细阅读下列三段文字:
①由稀有气体元素Xe(氙)与氧元素形成的一种共价化合物XeO3极不稳定,易转化为单质而呈强氧化性。将适量的XeO3投入含Mn2+的水溶液中,溶液逐渐变为紫红色且pH不断减小。
②将0.08 mol KMnO4固体(质量为12.64 g)加热一段时间后,收集到a mol O2;向反应后残留的固体中加入足量的浓盐酸,又收集到b mol Cl2,此时Mn元素全部以Mn2+的形式存在于溶液中。
③氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
Cl2+2e-===2Cl-。
回答问题:
(1)试写出①有关的离子方程式:____________________________________________。
(2)请配平②的化学方程式:
________KMnO4+________HCl——________KCl+________MnCl2+________Cl2↑+________H2O
通过对第②段文字中提供的数据进行计算可得出:a+b的最大值为________,a+b最小值为________。
(3)下列四种物质中能使③中的还原过程发生的物质是________。
A.Na2CO3 B.KMnO4
C.XeO3  D.Na2SO3
D.Na2SO3
将该反应的氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并用单线桥表示电子转移的方向和数目:
 +
+
查看答案和解析>>
科目:高中化学 来源: 题型:
绿色化学实验是在绿色化学思想指导下的实验新方法,以减少污染、防止浪费等。下列符合绿色化学实验的是( )
A.用铜与浓硫酸反应制取CuSO4,并用少量品红溶液吸收尾气
B.将CO还原Fe2O3后的尾气直接排入空气中
C.用CCl4完成萃取操作练习时,将溴水改成碘水
D.将Zn和稀硫酸制H2后的废液倒入水槽后再清洗玻璃仪器
查看答案和解析>>
科目:高中化学 来源: 题型:
在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是
( )
A.pH=3的硝酸和pH=11的氢氧化钾溶液
B.pH=3的盐酸和pH=11的氨水
C.pH=3的硫酸和pH=11的氢氧化钠溶液
D.pH=3的醋酸和pH=11的氢氧化钡溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
形成节约能源和保护生态环境的产业结构是人类与自然和谐发展的重要保证,你认为下列行为中有悖于这一保证的是 ( )
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.沼气是可再生的二次能源, 可在农村推广使用
D.减少资源消耗、增加资源的重复使用和资源的循环再生
查看答案和解析>>
科目:高中化学 来源: 题型:
某金属氯化物MCl2 40.5g,含有0.600mol Cl-,则金属M的摩尔质量为 ( )
A. 135 B. 64 g·mol-1 C. 64 D. 135 g·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com