
氯碱工业电解所用的氯化钠溶液需精制。除去有影响的Ca2+、Mg2+、NH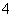 、SO
、SO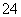 及泥沙,其精制流程如下:
及泥沙,其精制流程如下:
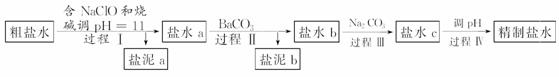 已知:①Ca2+、Mg2+开始形成相应氢氧化物沉淀的pH如下表。
已知:①Ca2+、Mg2+开始形成相应氢氧化物沉淀的pH如下表。
| Ca(OH)2 | Mg(OH)2 | |
| pH | ≥11.5 | ≥4.2 |
②Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=2.6×10-9,Ksp(CaCO3)=5.0×10-9。
下列说法正确的是( )
A.盐泥a除泥沙外,还含有Ca(OH)2和Mg(OH)2
B.过程Ⅰ中将NH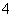 转化为N2的离子方程式是3ClO-+2NH
转化为N2的离子方程式是3ClO-+2NH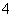 ===3Cl-+N2↑+3H2O+2H+
===3Cl-+N2↑+3H2O+2H+
C.过程Ⅱ中通入CO2有利于除SO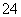
D.过程Ⅳ调pH可以使用硝酸
科目:高中化学 来源: 题型:
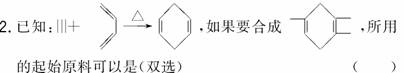
A.2甲基1,3丁二烯和2丁炔
B.1,3戊二烯和2丁炔
C.2,3二甲基1,3戊二烯和乙炔
D.2,3二甲基1,3丁二烯和丙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
烧杯A中盛放0.1 mol/L的H2SO4溶液,烧杯B中盛放0.1 mol/L的CuCl2溶液(两种溶液均足量),组成的装置如图所示。下列说法不正确的是( )
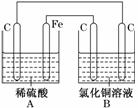
A.A为原电池,B为电解池
B.A为电解池,B为原电池
C.当A烧杯中产生0.1 mol气体时,B烧杯中产生气体的物质的量也为0.1 mol
D.经过一段时间,B烧杯中溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇脱氢可制取甲醛CH3OH(g)HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示(已知反应在1 L的密闭容器中进行)。下列有关说法正确的是( )
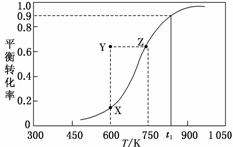
A.脱氢反应的ΔH<0
B.600 K时,Y点甲醇的v逆<v正
C.从Y点到Z点可通过增大压强
D.在t1 K时,该反应的平衡常数为8.1
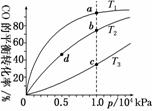
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下反应,①NH3+H+NH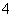 (平衡常数为K1),②Ag++Cl-AgCl(平衡常数为K2),③Ag++2NH3Ag(NH3)
(平衡常数为K1),②Ag++Cl-AgCl(平衡常数为K2),③Ag++2NH3Ag(NH3)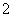 (平衡常数为K3)。①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是( )
(平衡常数为K3)。①、②、③的平衡常数关系为K1>K3>K2,据此所做的以下推测合理的是( )
A.氯化银不溶于氨水
B.银氨溶液中加入少量氯化钠有白色沉淀
C.银氨溶液中加入盐酸有白色沉淀
D.银氨溶液可在酸性条件下稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6g硫化氢④0.2mol NH3.下列对这四种气体的关系从小到大表示不正确的是()
| A. | 体积:④<①<②<③ | B. | 密度:①<④<③<② | |
| C. | 质量:④<①<③<② | D. | 氢原子数:②<④<③<① |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C三种物质各15g,发生如下反应:A+B+C→D反应后生成D的质量为30g.然后在残留物中加入10g A,反应又继续进行,待反应再次停止,反应物中只剩余C,则下列说法正确的是()
| A. | 第一次反应停止时,剩余B 9 g | |
| B. | 第一次反应停止时,剩余C 6 g | |
| C. | 反应中A和C的质量比是5:3 | |
| D. | 第二次反应后,C剩余5 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于氧化还原反应的是()
| A. | CaCO3 | |
| B. | Na2CO3+2HCl═2NaCl+CO2↑+H2O | |
| C. | 2Cu+O2 | |
| D. | Fe2O3+3H2SO4═Fe2(SO4)3+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
CH4气体的燃烧热△H= -802kJ• mol-1,当CH4不完全燃烧生成CO气体和液态
H2O时,放出的热量为519 kJ。如果1 mol CH4与n g O2燃烧生成CO、CO2气体和液
态H2O,放出731.25 kJ热量。
(1)写出CH4气体不完全燃烧的热化学方程式。
(2)计算n的值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com