
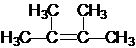 Ćū³ĘĪŖ2£¬3-¶ž¼×»ł-2-¶”Ļ©
Ćū³ĘĪŖ2£¬3-¶ž¼×»ł-2-¶”Ļ©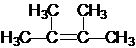 ”ś
”ś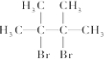
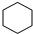 £®
£® ·ÖĪö £Ø1£©Ä³ĢžAµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ84£¬ŌņĢžÖŠCŌ×Ó×ī“óŹżÄæ=$\frac{84}{12}$=7£¬¹ŹÓŠ»śĪļ·Ö×ÓŹ½ĪŖC6H12£»
£Ø2£©ĢžµÄĶØŹ½ĪŖCxHy£¬Čō×ÜĪļÖŹµÄĮæŅ»¶Ø£¬Čōø÷×é·ÖŗÄŃõĮæ£Øx+$\frac{y}{4}$£©ĻąµČ£¬ŌņĻūŗÄŃõĘųµÄĮæĻąµČ£»Čō×ÜÖŹĮæŅ»¶Ø£¬³ä·ÖČ¼ÉÕĻūŗÄŃõĘųµÄĮæ²»±ä£¬Į½ÖÖĢžµÄ×ī¼ņŹ½ĻąĶ¬£»
£Ø3£©¢ŁČōĢžAĪŖĮ“Ģž£¬Ó¦ŗ¬ÓŠŅ»øöĢ¼Ģ¼Ė«¼ü£¬·Ö×ÓÖŠĖłÓŠµÄĢ¼Ō×ÓŌŚĶ¬Ņ»Ę½ĆęÉĻ£¬øĆ·Ö×ÓµÄŅ»ĀČČ”“śĪļÖ»ÓŠŅ»ÖÖ£¬Ö»ÓŠ1ÖÖĒāŌ×Ó£»
¢ŚAĪŖĻ©Ģž£¬1molAÓė1molµ„ÖŹäå·¢Éś¼Ó³É·“Ӧɜ³É¶žäå“śĪļ£»
¢ŪÓėA»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬ĒŅÖ÷Į“Ģ¼Ō×ÓøöŹżÓėAĻąĶ¬µÄĮ“ĢžÓŠ£ŗCH2=C£ØCH2£©CH£ØCH3£©2£¬CH2=CHC£ØCH3£©3£¬CH2=C£ØCH2CH3£©2£»
£Ø4£©A²»ÄÜŹ¹äåĖ®ĶŹÉ«£¬ĒŅĘäŅ»ĀČ“śĪļÖ»ÓŠŅ»ÖÖ£¬Ōņ²»ŗ¬C=C£¬Ö»ÓŠŅ»ÖÖH£¬Ó¦ĪŖ»·Ģž
½ā“š ½ā£ŗ£Ø1£©Ä³ĢžAµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ84£¬ŌņĢžÖŠCŌ×Ó×ī“óŹżÄæ=$\frac{84}{12}$=7£¬ŅņĪŖĢžÖŠ»¹ŗ¬ÓŠHŌŖĖŲ£¬ĖłŅŌCŌ×ÓŹżÄæĪŖ6£¬ŌņHŌ×ÓŹżĪŖ$\frac{84-12”Į6}{1}$=12£¬¹ŹÓŠ»śĪļ·Ö×ÓŹ½ĪŖC6H12£»
¹Ź“š°øĪŖ£ŗC6H12£»
£Ø2£©ĢžµÄĶØŹ½ĪŖCxHy£¬Čō×ÜĪļÖŹµÄĮæŅ»¶Ø£¬Čōø÷×é·ÖŗÄŃõĮæ£Øx+$\frac{y}{4}$£©ĻąµČ£¬ŌņĻūŗÄŃõĘųµÄĮæĻąµČ£¬·ńŌņ²»ĻąµČ£¬C6H12µÄŗÄŃõĮæĪŖ9£¬C7H8 µÄŗÄŃõĮæĪŖ9£¬ĖłŅŌ¶žÕß
×ÜĪļÖŹµÄĮæŅ»¶Ø£¬³ä·ÖČ¼ÉÕĻūŗÄŃõĘųµÄĮæ²»±ä£»
Čō×ÜÖŹĮæŅ»¶Ø£¬³ä·ÖČ¼ÉÕĻūŗÄŃõĘųµÄĮæ²»±ä£¬Į½ÖÖĢžµÄ×ī¼ņŹ½ĻąĶ¬£¬C6H12µÄ×ī¼ņŹ½ĪŖCH2£¬C7H14µÄ×ī¼ņŹ½ĪŖCH2£»
¹Ź“š°øĪŖ£ŗA£»C£»
£Ø3£©¢ŁČōĢžAĪŖĮ“Ģž£¬Ó¦ŗ¬ÓŠŅ»øöĢ¼Ģ¼Ė«¼ü£¬·Ö×ÓÖŠĖłÓŠµÄĢ¼Ō×ÓŌŚĶ¬Ņ»Ę½ĆęÉĻ£¬øĆ·Ö×ÓµÄŅ»ĀČČ”“śĪļÖ»ÓŠŅ»ÖÖ£¬ŌņAĪŖ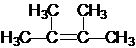
¹Ź“š°øĪŖ£ŗ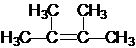
¢ŚAĪŖĻ©Ģž£¬1molAÓė1molµ„ÖŹäå·¢Éś¼Ó³É·“Ӧɜ³É¶žäå“śĪļ£¬Ęä·“Ó¦·½³ĢŹ½ĪŖ£ŗBr2+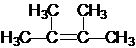
 £»
£»
¹Ź“š°øĪŖ£ŗBr2+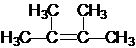
 £»
£»
¢ŪÓėA»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬ĒŅÖ÷Į“Ģ¼Ō×ÓøöŹżÓėAĻąĶ¬µÄĮ“ĢžÓŠ£ŗCH2=C£ØCH2£©CH£ØCH3£©2£¬CH2=CHC£ØCH3£©3£¬CH2=C£ØCH2CH3£©2£¬ŌņAµÄĶ¬·ÖŅģ¹¹ĢåŹżÄæĪŖ3£»
¹Ź“š°øĪŖ£ŗ3£»
£Ø4£©ČōA²»ÄÜŹ¹äåĖ®ĶŹÉ«£¬ĒŅĘäŅ»ĀČ“śĪļÖ»ÓŠŅ»ÖÖ£¬ŌņAĪŖ»·¼ŗĶ飬½į¹¹¼ņŹ½ĪŖ£ŗ £»
£»
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ”¢ÓŠ»śĪļČ¼ÉÕŗÄŃõĮæĪŹĢā”¢ĻŽÖĘĢõ¼žĶ¬·ÖŅģ¹¹ĢåŹéŠ“µČ£¬ĢāÄæ±Č½Ļ×ŪŗĻ£¬ŹĒ¶Ō»ł“”ÖŖŹ¶µÄ×ŪŗĻ漲飬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
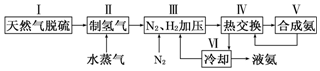
| A£® | ·“Ó¦¢ŁÖŠµēÄÜ×Ŗ»ÆĪŖ»ÆѧÄÜ | |
| B£® | ·“Ó¦¢ŚĪŖ·ÅČČ·“Ó¦ | |
| C£® | ·“Ó¦¢ŪŹ¹ÓĆ“ß»Æ¼Į£¬”÷H3¼õŠ” | |
| D£® | ·“Ó¦CH4£Øg£©=C£Øs£©+2H2£Øg£©µÄ”÷H=+74.8 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢Mg2+”¢CO32-”¢I- | B£® | H+”¢NO3-”¢Fe2+”¢Br- | ||
| C£® | NH4+”¢K+”¢SO42-”¢Cl- | D£® | Na+”¢S2-”¢Cu2+”¢SO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼ÓČėÉŁĮæNa2CO3¹ĢĢå£¬Ę½ŗā¢ŁÓŅŅĘ£¬Ę½ŗā¢Ś×óŅĘ£¬ČÜŅŗÖŠc£ØF-£©Ōö“ó | |
| B£® | ¼ÓČėÉŁĮæNaOH¹ĢĢåÖĮc£ØF-£©£¾c£ØHF£©£¬ČÜŅŗŅ»¶Ø³Ź¼īŠŌ | |
| C£® | ¼ÓČėÉŁĮæNaÖĮpH=8£¬ŌņC£ØNa+£©-c£ØF-£©=0.99”Į10-7mol•L-1 | |
| D£® | ¼ÓČėÉŁĮæŃĪĖį£¬$\frac{c£Ø{F}^{-}£©}{c£ØHF£©•c£ØO{H}^{-}£©}$²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
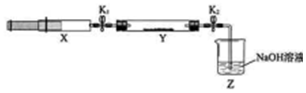
| ²Ł×÷²½Öč | ŹµŃéĻÖĻó | ½āŹĶŌŅņ |
| “ņæŖK1£¬ĶʶÆ×¢ÉäĘ÷»īČū£¬Ź¹XÖŠµÄĘųĢå»ŗĀżĶØČėY¹ÜÖŠ | ¢ŁY¹ÜÖŠŗģ×ŲÉ«ĘųĢåĀżĀż±äĒ³ | ¢Ś·“Ó¦µÄ»Æѧ·½³ĢŹ½ 8NH3+6NO2 $\frac{\underline{\;“߻ƼĮ\;}}{\;}$7N2+12H2O |
| ½«×¢ÉäĘ÷»īČūĶĖ»ŲŌ“¦²¢¹Ģ¶Ø£¬“ż×°ÖĆ»Öø“µ½ŹŅĪĀ | Y¹ÜÖŠÓŠÉŁĮæĖ®Öé | Éś³ÉµÄĘųĢ¬Ė®Äż¼Æ |
| “ņæŖK2 | ¢ŪZÖŠNaOHČÜŅŗ²śÉśµ¹ĪüĻÖĻó | ¢Ü·“Ó¦ŗóĘųĢå·Ö×ÓŹż¼õÉŁ£¬Y¹ÜÖŠŃ¹ĒæŠ”ÓŚĶāŃ¹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| µĪ¶Ø“ĪŹż | “ż²āŅŗĢå»ż £ØmL£© | ±ź×¼KMnO4ČÜŅŗĢå»ż£ØmL£© | |
| µĪ¶ØĒ°¶ĮŹż | µĪ¶Øŗó¶ĮŹż | ||
| µŚŅ»“Ī | 25.00 | 0.50 | 20.40 |
| µŚ¶ž“Ī | 25.00 | 3.00 | 23.00 |
| µŚČż“Ī | 25.00 | 4.00 | 24.10 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com