
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合溶液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )
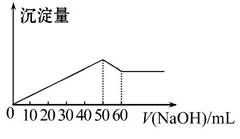
A.6∶1 B.3∶1 C.2∶1 D.1∶2
 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
某气体的摩尔质量为M g·mol-1,分子数目为N,质量是m g,阿伏加德罗常数为NA,m(C)为一个12C的质量,试说明下列各式所表示的意义。
(1)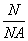 :__________________________________________________________。
:__________________________________________________________。
(2)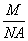 :______________________________________________________________。
:______________________________________________________________。
(3)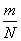 :_______________________________________________________________。
:_______________________________________________________________。
(4)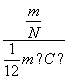 :____________________________________________________________。
:____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.硝酸银与盐酸反应:
AgNO3+Cl-====AgCl↓+N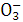
B.铜片插入硝酸银溶液中:Cu+Ag+====Ag+Cu2+
C.硫酸和氯化钡溶液反应:Ba2++S ====BaSO4↓
====BaSO4↓
D.铁钉放入硫酸铜溶液中: 2Fe+3Cu2+====2Fe3++3Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了下列4种不同的方法,其中不可行的是( )
A.分别加入等量水中,看溶解能力差异
B.分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊
C.分别取样配成溶液,滴加Ba(OH)2溶液,观察有无白色沉淀
D.分别配成溶液,用铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 小苏打可用于治疗胃病 | NaHCO3可与盐酸反应 | Ⅰ对,Ⅱ对,有 |
| B | 向Na2O2的水溶液中滴入酚酞变红色 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错,无 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
| D | 过氧化钠可用作航天员的供氧剂 | Na2O2能和CO2、H2O反应生成O2 | Ⅰ对,Ⅱ对,有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,回答下列有关问题:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)在①~⑫元素中,金属性最强的元素是________,非金属性最强的元素是________,最不活泼的元素是________。(均填元素符号)
(2)元素⑦与元素⑧相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(3)第3周期中原子半径最大的元素是________(填元素符号),跟它同周期的原子半径最小的元素是________(填元素符号),它们可以形成的化合物的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2 + Pb + 2H2SO4 = 2PbSO4↓ + 2H2O,根据此反应判断下列叙述中正确的是( )
A.PbO2是电池的负极
B.负极的电极反应式为:Pb + SO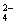 – 2e – = PbSO4↓
– 2e – = PbSO4↓
C.PbO2得电子,被氧化
D.电池放电时,溶液酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家根据元素周期律和原子结构理论预测,原子序数为114的元素位于第7周期ⅣA族,称为类铅元素。下面关于它的原子结构和性质预测正确的是( )
A.类铅元素原子的最外层电子数为6
B.其常见价态为+4、-4
C.它的金属性比铅强
D.它的原子半径比铅小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com