分析:①工业上用氨气(NH
3)制取硝酸(HNO
3),工业流程为:4NH
3+5O
2 4NO+6H
2O、2NO+O
2=2NO
2 、3NO
2+H
2O=2HNO
3+NO;
②工业上常以食盐为原料制备氯气,再用氯气制备漂白粉:①2NaCl+2H
2O
2NaOH+H
2↑+Cl
2↑,②2C1
2+2Ca(OH)
2=CaCl
2+Ca(ClO)
2+2H
2O;
③工业上制Mg的过程:MgC1
2溶液:将MgC1
2溶液经蒸发结晶得到MgC1
2?6H
2O,然后MgC1
2?6H
2O在一定条件下加热得到无水MgC1
2:MgCl
2?6H
2O
MgCl
2+6H
2O;最后电解熔融的氯化镁可得到Mg:MgCl
2Mg+Cl
2↑;
④联合制碱法:先使氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,其化学反应原理是:NH
3+CO
2+H
2O+NaCl(饱和)=NaHCO
3↓+NH
4Cl,将经过滤、洗涤得到的NaHCO
3微小晶体,再加热煅烧制得纯碱产品:2NaHCO
3Na
2CO
3+CO
2↑+H
2O;
⑤从铝土矿中提取铝反应过程 ①溶解:将铝土矿溶于NaOH(aq):Al?O?+2NaOH=2NaAlO+H?O ②过滤:除去残渣氧化亚铁(FeO)、硅铝酸钠等 ③酸化:向滤液中通入过量CO
2:
NaAlO
2+CO?+2H?O=Al(OH)?↓+NaHCO?④过滤、灼烧 Al(OH)?:2Al(OH)?
Al
2O
3+3H?O; ⑤电解:2Al
2O
3(l)
4Al+3O?↑.



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 NO
NO  HNO3
HNO3 Cl2
Cl2  漂白粉
漂白粉 无水MgCl2
无水MgCl2  Mg
Mg NaHCO3
NaHCO3  Na2CO3
Na2CO3 NaAlO2溶液
NaAlO2溶液 Al(OH)3
Al(OH)3 Al2O3
Al2O3  Al
Al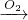 NO
NO HNO3
HNO3 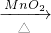 Cl2
Cl2 漂白粉
漂白粉  无水MgCl2
无水MgCl2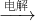 Mg
Mg 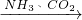 NaHCO3
NaHCO3 Na2CO3
Na2CO3 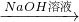 NaAlO2溶液
NaAlO2溶液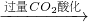 Al(OH)3
Al(OH)3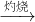 Al2O3
Al2O3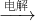 Al.
Al.![]() NO
NO ![]() HNO3
HNO3![]() Cl2
Cl2 ![]() 漂白粉
漂白粉![]() 无水MgCl2
无水MgCl2 ![]() Mg
Mg![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3![]() NaAlO2溶液
NaAlO2溶液![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3 ![]() Al
Al