
分析 结构简式就是结构式的简单表达式:只要把碳氢单键省略掉即可,碳碳单键可以省略也可不省略,但是碳碳双键、三键一定不能省略,碳氧双键可省略;根据名称与结构简式的对应关系和书写结构方法来写.
解答 解:(1)2,4-二甲基-3,3-二乙基己烷的主链为6个C,2号位和4号位上各含有1个甲基,3号位有2个乙基,其结构简式为CH3CH(CH3)C(CH2CH3)2CH(CH3)CH2CH3;
故答案为:CH3CH(CH3)C(CH2CH3)2CH(CH3)CH2CH3;
(2)2,3,5-三甲基-3,4,4-三乙基辛烷的主链为8个C,2号位和3号位上和5号位上各含有1个甲基,3号位有1个乙基,4号位有2个乙基,其结构简式为CH3CH(CH3)C(CH3)(CH2CH3)C(CH2CH3)2CH(CH3)CH2CH2CH3,故答案为:CH3CH(CH3)C(CH3)(CH2CH3)C(CH2CH3)2CH(CH3)CH2CH2CH3.
点评 本题考查结构简式的书写,题目难度中等,注意只要把碳氢单键省略掉即可,碳碳单键可以省略也可不省略,但是碳碳双键、三键一定不能省略,碳氧双键可省略.


科目:高中化学 来源: 题型:选择题
| A. | 3v正(N2)=v正(H2) | B. | v正(N2)=v逆(NH3) | C. | 2v正(H2)=3v逆(NH3) | D. | v正(N2)=3v逆(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硝酸盐是还原剂 | B. | 维生素C是还原剂 | ||
| C. | 维生素C是氧化剂 | D. | 亚硝酸盐被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 投入铁片产生H2的溶液中可大量存在H+,Mg2+,SO${\;}_{4}^{2-}$,NO${\;}_{3}^{-}$ | |
| B. | 可用稀硝酸除去试管内壁上的银镜 | |
| C. | 1.0mol•L-1的KNO3溶液中可大量存在H+,Fe2+,Cl-,SO${\;}_{4}^{2-}$ | |
| D. | 硫化铜溶于硝酸的离子方程式为CuS+2H+═H2S↑+Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
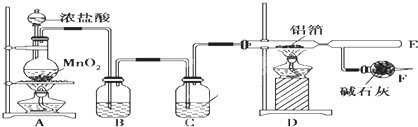
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 Fe(OH)3+3H+,过量盐酸抑制FeCl3水解(结合离子方程式简要说明).
Fe(OH)3+3H+,过量盐酸抑制FeCl3水解(结合离子方程式简要说明).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加酶洗衣粉洗衣服时,温度越高效果越好 | |
| B. | “神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 | |
| C. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| D. | 乙二醇可用来生产聚酯纤维和作汽车发动机的抗冻剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com