
【题目】β一受体阻滞剂盐酸艾司洛尔(F)的一种合成路线如下:
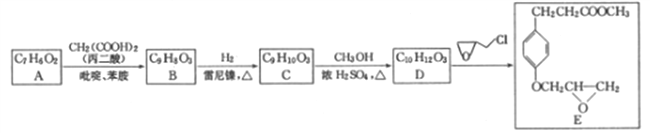
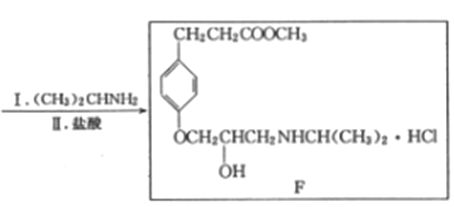
已知: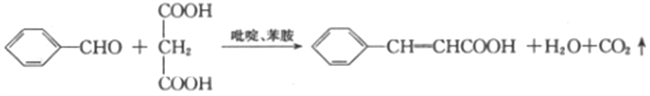
回答下列问题:
(1)A的化学名称是____________;F中含氧官能团的名称是___________________。
(2)由B生成C的反应类型为____________,由D生成E的反应类型为____________。
(3)B的结构简式为____________。
(4)由C生成D的化学方程式为____________。
(5)三取代芳香族化合物X是E的同分异构体,1molX与足量的NaHCO3反应可生成44.8L(标准状况)CO2,其核磁共振氢谱显示有5种不同化学环境的氢,且其峰面积之比为9:2:2:2:1。写出2种符合要求的X的结构简式:________________________________________________。
(6)写出以苯甲醇和丙二酸为原料制备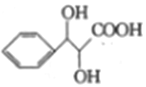 的合成路线_____________(其他无机试剂任选)。
的合成路线_____________(其他无机试剂任选)。
【答案】 对羟基苯甲醛(4-羟基苯甲醛) 醚键、羟基和酯基 加成反应 取代反应 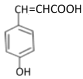
 、
、
![]()
![]()
![]()
![]()
![]()
![]()
![]()
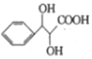
【解析】由流程中D→E的反应情况,结合E的结构简式和D的分子式,可得D→E发生取代反应,D的结构简式为: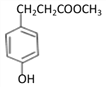 ;由C→D的反应条件,结合C和D的分子式,可得C→D发生酯化反应,C的结构简式为:
;由C→D的反应条件,结合C和D的分子式,可得C→D发生酯化反应,C的结构简式为: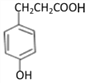 ;B与氢气一定条件下反应生成C,结合B、C的分子式及C的结构简式,可得B→C发生加成反应,B的结构简式为:
;B与氢气一定条件下反应生成C,结合B、C的分子式及C的结构简式,可得B→C发生加成反应,B的结构简式为: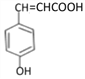 ;由A、B的分子式及B的结构简式,结合已知中苯甲醛和丙二酸的反应,可得A的结构简式为:
;由A、B的分子式及B的结构简式,结合已知中苯甲醛和丙二酸的反应,可得A的结构简式为:![]() 。
。
(1)由上述分析,A的结构简式为:![]() ,化学名称是:对羟基苯甲醛(或4-羟基苯甲醛);由F的结构简式可得,F中含氧官能团的名称是:醚键、羟基和酯基。
,化学名称是:对羟基苯甲醛(或4-羟基苯甲醛);由F的结构简式可得,F中含氧官能团的名称是:醚键、羟基和酯基。
(2)由上述分析知,B→C反应类型为:加成反应;由D生成E的反应类型为:取代反应。
(3)由上述分析知,B的结构简式为: 。
。
(4)C为: 、D为:
、D为: ,C与甲醇发生酯化反应生成D,化学方程式为:
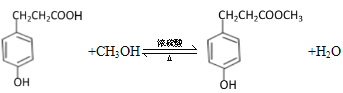
,C与甲醇发生酯化反应生成D,化学方程式为: +CH3OH
+CH3OH![]()
 +H2O。
+H2O。
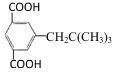
(5)E为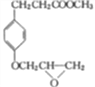 ,三取代芳香族化合物X是E的同分异构体,1molX与足量的NaHCO3反应可生成44.8L(标准状况)CO2,则X中有2个羧基;X核磁共振氢谱显示有5种不同化学环境的氢,且其峰面积之比为9:2:2:2:1,则X可以是:
,三取代芳香族化合物X是E的同分异构体,1molX与足量的NaHCO3反应可生成44.8L(标准状况)CO2,则X中有2个羧基;X核磁共振氢谱显示有5种不同化学环境的氢,且其峰面积之比为9:2:2:2:1,则X可以是: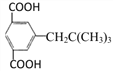 、
、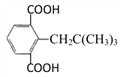 。
。
(6)由已知: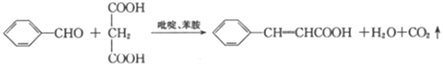 得到启发,以苯甲醇和丙二酸为原料制备
得到启发,以苯甲醇和丙二酸为原料制备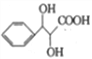 ,可以先催化氧化苯甲醇(
,可以先催化氧化苯甲醇(![]() )为苯甲醛(
)为苯甲醛(![]() ),然后发生类似上述反应生成
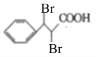
),然后发生类似上述反应生成![]() ,再与溴单质发生加成反应生成
,再与溴单质发生加成反应生成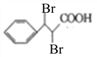 ,最后水解生成
,最后水解生成 ,故流程为:
,故流程为:![]()
![]()
![]()
![]()
![]()
![]()

![]()
 。
。


科目:高中化学 来源: 题型:
【题目】已知A为常见的金属单质,根据下图所示的关系,回答下列问题。
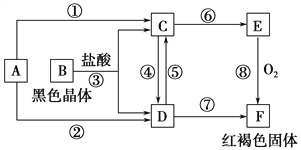
(1)确定A、B、C、D、E、F的化学式,A为________,B为________,C为________,D为________,E为________,F为________。
(2)写出反应⑧的化学方程式和反应④、⑤的离子方程式。
⑧_____________________________________________________;
④_____________________________________________________;
⑤_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,分析其元素的填充规律,判断下列说法正确的是( )
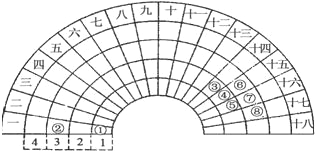
A. ③元素形成的单质晶体均属于原子晶体
B. ④元素的气态氢化物易液化,是因为其分子间存在氢键
C. ②、⑦、⑧对应的简单离子半径依次减小
D. ②⑤⑦三种元素形成的盐溶液在 25℃时的 pH值为7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)Br位于元素周期表第_____周期第_____族;基态Na+核外有_____种运动状态不同的电子;Mg基态原子核外电子排布式为_____。
(2)用“>”或“<”填空:
第一电离能 | 粒子半径 | 熔点 | 键的极性 |
N_____S | S2—_____ Mg2+ | SO3______Na2O2 | H﹣O_____H﹣N |
(3)已知多硫化钠﹣溴储能电池是一种二次电池,结构如图。电池总反应为:2Na2S3+2NaBr![]() 3Na2S2+Br2。
3Na2S2+Br2。
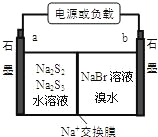
①放电时Na+向_____极迁移(填“a 或 b”);
②充电时阴极电极反应式为:______________。
(4)已知N4为正四面体结构,N﹣N键能为167kJ/mol,N≡N 键能为 942kJ/mol。写 出N4(g)转化为N2(g)的热化学方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用软锰矿(主要成分为MnO2)来制取硫酸锰,工艺流程如下:
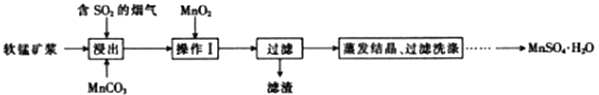
已知:浸出液中的金属离子主要是Mn2+,还含有少量的Fe2+。回答下列问题:
(1)实验室进行过滤操作时用到的玻璃仪器有玻璃棒、_____________________。
(2)操作Ⅰ的目的是_______________________和调节溶液的PH至3~4。检验过滤后的滤液中是否含有Fe3+的操作是___________________________________________________________________。
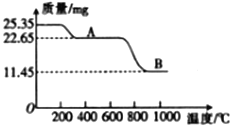
(3)通过煅烧MnSO4·H2O可制得软磁铁氧体材料(MnxO4),在不同温度下煅烧MnSO4·H2O时剩余质量变化的曲线如图所示。根据图中数据可得MnxO4中x的值为______________。A到B过程中分解得到的气体中SO2与SO3的物质的量之比为2∶1,写出该过程中发生反应的化学方程式:______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生活生产中常见的物质里含有的有机物属于高分子化合物的是
A. 植物中所含的非常复杂的叶绿素 B. 石油分馏所得的重油中含有的C16H34
C. 植物油水解得到的高级脂肪酸 D. 芹菜中含有的粗糙的纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国女药学家屠呦呦因创制新型抗疟药——青蒿素(结构如图)和双氢青蒿素的贡献,挽救了全球特别是发展中国家的数百万人的生命”。青蒿素是从植物黄花蒿茎叶中提取的,荣获2015年诺贝尔奖生物学或医学奖。下列有关青蒿素的叙述不正确的是

A. 分子式为C15H22O5
B. 它在乙醚中的溶解度大于在水中的溶解度
C. 能发生取代反应、水解反应、加成反应,不能发生氧化反应
D. 该物质不稳定,容易受到热和还原性物质的影响而发生变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿是一种重要的化工原料,主要成分是CuFeS2,另外还有少量的氧化铝、二氧化硅及水分,通过化学工艺可获得许多化工产品。
(1)铜元素位于元素周期表中_________(填写周期、族);基态Fe原子的价层电子轨道表达式为_____;
(2)硫位于第VIA 族,该族元素氢化物沸点由低到高的顺序及原因是_________(必要化学用语及文字简答)。
(3)基态氮原子的第一电离能大于氧原子的第一电离能的原因是__________。
(4)由铝和氯元素组成的化合物熔点190℃、在熔融态不导电;该化合物易升华,其蒸气密度是相同条件下氢气的133.5倍。请写出其蒸气分子的结构式______________(如有配位键,请 用“→”表 示 )。(5)黄铜矿在空气中高温灼烧可以得到固体混合物和废气,固体混合物中有X和Y两化合物。固体化合物X的晶胞模型如图甲所示:
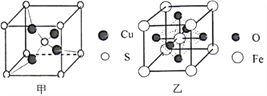
①化合物X的化学式:___________;
②废气中SO2经催化氧化生成SO3,SO3分子中硫原子杂化方式为___________;SO3分子空间构型是___________。
(6)黄铜矿高温灼烧得到的另一固体化合物Y的晶胞模型如图乙,已知丫晶体密度为ρg/cm3,则Y 晶体中晶胞边长是_____cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种有机物有如下转化关系。已知B可以发生银镜反应,D气体密度是氢气的14倍。

根据图示,
(1)试写出A、C、E的结构简式:A_____、C_______、E________。
(2)写出下列反应的化学方程式:
A→D:_______________________;
A→B: _______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com