
| A. | 常温下都是液体 | B. | 都能在空气中燃烧 | ||
| C. | 都能使酸性高锰酸钾溶液褪色 | D. | 都能发生取代反应 |
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W |
| A. | Y元素的气态氢化物易液化,是因为其分子间能形成氢键 | |
| B. | X元素最高价氧化物分子的比例模型为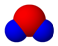 | |
| C. | Z单质与X元素最高价氧化物、Y单质都能反应,体现氧化性 | |
| D. | W的单质在地壳含量丰富,工业上可通过电解它的无水盐来制备 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2摩尔质量是60 | |
| B. | 1 molSiO2中含有1 molO2 | |
| C. | 1.5 molSiO2中含有1.806×1024个氧原子 | |
| D. | 1 molSiO2质量是60 g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
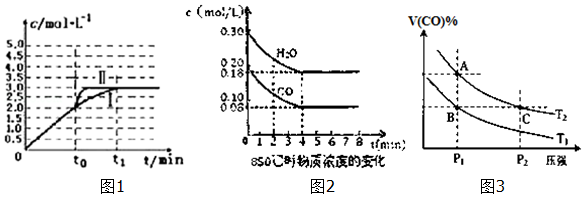
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
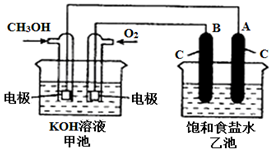 甲醇是一种可再生能源,具有广泛的开发和应用前景.如图是用甲醇燃料电池电解饱和食盐水的装置示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.
甲醇是一种可再生能源,具有广泛的开发和应用前景.如图是用甲醇燃料电池电解饱和食盐水的装置示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 140℃时,无水乙醇与浓硫酸共热可制备乙烯 | |
| B. | 往油脂中加稀硫酸与之共热可发生皂化反应 | |
| C. | 可用碘溶液检验淀粉是否水解完全 | |
| D. | 验证溴乙烷中的溴元素,可直接加AgNO3溶液观察是否有淡黄色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3+HCl═NaCl+H2O+CO2↑ | B. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$ 2KCl+2O2↑ | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | 2CuO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com