
利用下列实验装置不能完成相应实验的是 ( )。
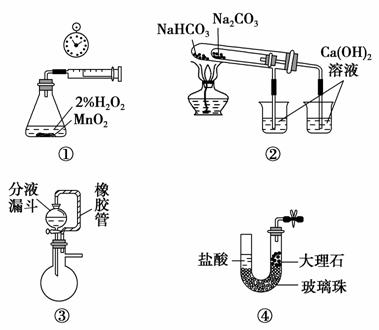
A.用装置①测量生成氧气的化学反应速率
B.用装置②比较NaHCO3和Na2CO3的热稳定性
C.装置③中分液漏斗内的液体可顺利加入蒸馏烧瓶中
D.装置④可实现制取CO2实验中的“即关即止,即开即用”的作用
科目:高中化学 来源: 题型:
下面有关晶体的叙述中,不正确的是 ( )
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现进行下列两个实验:(N2O4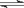 2NO2 △H > 0)
2NO2 △H > 0)
(a)将两容器置于沸水中加热
(b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是
A.(a)甲>乙,(b)甲>乙 B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿烧渣(含Fe2O3.SiO2.Al2O3等)转变成重要的工业原料FeSO4(反应条件略)
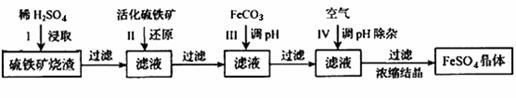
活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2( SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应,请回答下列问题:
SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其它反应,请回答下列问题:
(1)第1步H2SO4与Fe2O3反应的离子方程式是 。
(2)检验第II步中Fe3+是否完全还原,应选择 (填字母编号)。
A.KMnO4溶液 B.K3[Fe(CN)6]溶液 C.KSCN溶液
(3)第III步加FeCO3调溶液pH=6时,利用相关数据计算,判断Al3+是否沉淀完全? (填“是”或“否”)(已知Ksp【Al(OH)3】=1.9×10-33,当离子浓度小于1×10-5mol·L-1时,可认为沉淀完全)
(4)FeCO3在空气中加热反应可制得铁系氧化物材料。
已知25℃,101kPa时:4Fe(s)+3O2(g)=2Fe2O3(s) 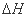 = —1648kJ/mol
= —1648kJ/mol
C(s)+O2(g)=CO2(g) 
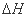 = —393kJ/mol
= —393kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) 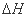
 = —1480kJ/mol
= —1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是 。
(5)FeSO4在一定条件下可制得F eS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li + FeS2 = Fe + 2Li2S,正极反应式是
eS2(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为4Li + FeS2 = Fe + 2Li2S,正极反应式是 
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
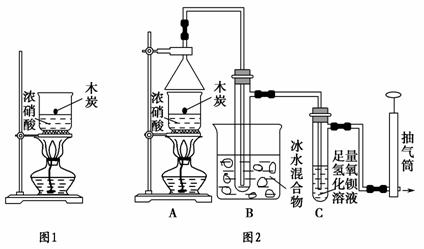
某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)乙同学认为甲同学的结论是错误的,他的理由是____________________ ________(用化学方程式表示),所以他认为应该检验________(填化学式)的产生来证明碳与浓硝酸发生了反应。为此乙同学查阅相关资料得知“0 ℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。
(2)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号)________。
①将炭与浓硝酸一同放在装置中加热;
②先加热浓硝酸,然后将炭投入其中;
③先加热炭,再加入冷浓硝酸;
④先加热炭,再将炭投入冷浓硝酸中。
(3)请用平衡移动原理解释B装置的作用_______________________________
_________________________________________________________________。
(4)C装置中出现的现象是______________,经检测C的溶液中还含有少量氮元素,只以NO 形式存在,写出生成该离子的化学方程式_________________。
形式存在,写出生成该离子的化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
0.6mol的Cu2S与足量的稀HNO3反应,生成物为Cu(NO3)2、H2SO4、NO、H2O,则参加反应的被还原和未被还原的硝酸的物质的量分别为( )
A.0.6mol、0.3mol B.1.2mol、0.6mol
C.2mol、0.6mol D.2mol、2.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.36LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入2.5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A 60mL B.240mL C.30mL D.120mL
查看答案和解析>>
科目:高中化学 来源: 题型:
合金有许多特点,如Na-K合金为液体,而Na和K的单质均为固体。据此,试推测:生铁、纯铁、碳三种物质中,熔点最低的是( )
A.纯铁 B.生铁 C.碳 D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com