
 在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀质量与加入NaOH溶液质量关系如图所示,试计算:
在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀质量与加入NaOH溶液质量关系如图所示,试计算:| 200g氢氧化钠溶液中NaOH的质量 |
| 200g |
| 5.8g |
| 58g/mol |
| 80 |
| a |
| 58 |
| 5.8 |
| 120 |
| b |
| 78 |
| 7.8 |
| 8g+12g |
| 200g |
| 40 |
| c |
| 78 |
| 7.8 |
| 8g+12g+4g |
| 10% |


 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
| A、乙炔 | B、1,3-丁二烯 |
| C、戊炔 | D、丙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
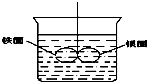 如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处,吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.
如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处,吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com