
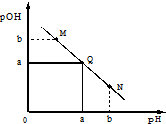
 某温度下,向一定体积0.1mol/LNaOH溶液中逐滴加入等浓度的CH3COOH溶液,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示,则下列说法错误的是( )
某温度下,向一定体积0.1mol/LNaOH溶液中逐滴加入等浓度的CH3COOH溶液,溶液中pOH[pOH=-lgc(OH-)]与pH的变化关系如图所示,则下列说法错误的是( )| A. | Q点消耗CH3COOH溶液的体积等于NaOH溶液的体积 | |
| B. | M、Q、N三点都满足:C(Na+)+C(H+)═c(CH3COO-)+C(OH-) | |
| C. | M点和N点所示溶液中水的电离程度相同 | |
| D. | N点所示溶液中c(CH3COO-)<c(Na+) |
分析 A.Q点pOH=pH,溶液显中性;
B.根据电荷守恒分析;
C.酸碱抑制水的电离,当氢离子与氢氧根离子浓度相同时,对水的抑制程度相同;
D.N点pH大于中性时的pH,溶液显碱性,结合电荷守恒分析.
解答 解:A.Q点pOH=pH,说明c(H+)═c(OH-),溶液显中性,当CH3COOH溶液的体积等于NaOH溶液的体积时,二者恰好完全反应生成CH3COONa,溶液显碱性,故A错误;
B.M、Q、N三点的溶液都存在电荷守恒,即:C(Na+)+C(H+)═c(CH3COO-)+C(OH-),故B正确;
C.酸碱抑制水的电离,当氢离子与氢氧根离子浓度相同时,对水的抑制程度相同,由图可知M、N点溶液中氢离子与氢氧根离子的浓度相同,所以M点和N点所示溶液中水的电离程度相同,故C正确;
D.N点pH大于中性时的pH,则溶液显碱性,所以c(H+)<c(OH-),溶液中电荷守恒C(Na+)+C(H+)═c(CH3COO-)+C(OH-),则c(CH3COO-)<c(Na+),故D正确.
故选A.
点评 本题考查酸碱中和的定性判断和计算,侧重于弱电解质的电离的考查,注意弱电解质的电离特点,把握pOH的含义,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 纯盐酸 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
| B | 冰醋酸 | 福尔马林 | 硫酸钡 | 亚硫酸 | 二氧化硫 |
| C | 油酯 | 淀粉 | 苛性钾 | 氢硫酸 | 碳酸钙 |
| D | 重水 | 纤维素 | 氯化钠 | 次氯酸 | 氯气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/pm | 160 | 143 | 112 | 104 | 66 |
| 主要化合价 | +2 | +3 | +2 | +6、+4、-2 | -2 |
| A. | 与稀盐酸反应的剧烈程度:L单质<Q单质 | |
| B. | 热稳定性:H2T<H2R | |
| C. | M与T形成的化合物具有两性 | |
| D. | L2+与R2-的核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应中,有两种离子化合物 | |
| B. | Mg3N2中,N3-的半径比Mg2+的半径大 | |
| C. | H2O与NH3含有相同的电子数,但H2O比NH3的稳定性差 | |
| D. | 碱性:Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下22.4 L NO与11.2 L O2混合后所得气体分子数为6.02×1023 | |
| B. | 标准状况下3.36 L CCl4含碳原子数为0.15×6.02×1023 | |
| C. | 1 mol甲基(-CH3)中所含电子数为9×6.02×1023 | |
| D. | 2 L 1 mol•L-1 的盐酸中所含氯化氢分子数为2×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入酸性KMnO4溶液,看紫红色是否褪去 |
| C | 分离Br2和CCl4混合物 | 向混合物中加入蒸馏水,然后分液 |
| D | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯原子的结构示意图: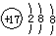 | |
| B. | N2的电子式: | |
| C. | CH4分子的比例模型: | |
| D. | 用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com