
光纤通信70年代后期发展起来的一种新型通信技术,目前长距离光纤通信系统已投入使用,光纤通信的光学纤维是由下列哪种物质经特殊工艺制成的()
A. 碳 B. 石英 C. 锗 D. 硅
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
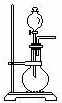
如图所示装置是实验室常用的一种制取气体的装置.
(1)下列制取气体的反应,可利用此装置进行制取有 (不一定是单选,多选漏选均不得分).
A、石灰石和稀硫酸反应制CO2 B、锌和稀盐酸反应制H2
C、MnO2催化双氧水分解制O2 D、KClO3和MnO2加热反应制取O2
(2)利用此装置制取H2并还原氧化铜,稀硫酸应该装在 中,写出H2还原氧化铜的反应方程式 ,由反应可说明H2的还原性 Cu(填“强于”、“弱于”).向装有8g CuO的试管中通入H2,若要使CuO全部被还原,则至少需要标准状况下的H2体积为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氧化性强弱顺序:Cl2>Br2>Fe3+>I2.下列反应或叙述不正确的是()
A. Br2+2HI=I2+2HBr
B. 2FeCl2+Cl2=2FeCl3
C. 2FeCl2+2HCl+I2=2FeCl3+2HI
D. 少量Cl2通入到NaBr和NaI的混合溶液中,Cl2优先氧化I﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
选择下列实验方法分离物质,将分离方法的序号填在横线上.
A、萃取分液法 B、加热分解C、结晶法D、分液法E、蒸馏法F、过滤法
(1) 分离饱和食盐水和沙子的混合物;
(2) 从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(3) 用四氯化碳从碘水中提取碘;
(4) 分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C),已知四氯化碳和甲苯互溶.
查看答案和解析>>
科目:高中化学 来源: 题型:
关于硝酸的说法正确的是()
A. 硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2
B. 浓HNO3与浓HCl按3:1的体积比所得的混合物叫王水
C. 硝酸与金属反应时,主要是+5价的氮元素得电子
D. 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中属于氧化还原反应,但水没有发生氧化还原反应的是()
A. Cl2+H2O=HCl+HClO B. 2F2+2H2O=4HF+O2
C. Na2O+H2O=2NaOH D. 2Na+H2O=2NaOH+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学﹣选修物质结构与性质]
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域.
单位质量的A和B单质燃烧时均放出大量热,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
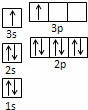
(1)某同学根据上述信息,推断B的核外电子排布如右图所示,
该同学所画的电子排布图违背了 .
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为 直 .
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C﹣C的键长为154.45pm,C60中C﹣C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 ,并阐述理由 .
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.写出基态钾原子的电子排布式 ,该物质的K原子和C60分子的个数比为 .
(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 N .Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为 .

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com