
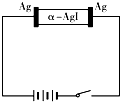
| A.阳极反应:Ag-e-═Ag+ |
| B.阴极质量不断增大 |
| C.若α-AgI是Ag+导电,则通电一段时间后晶体质量不变 |
| D.若α-AgI是Ag+导电,则通电一段时间后晶体质量减小 |
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.0.062(6.2%)19152 |
| B.0.062(6.2%)15219 |
| C.0.042(4.2%)1.29.4 |
| D.0.042(4.2%)9.41.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔融的NaCl(阳极) | B.NaCl溶液(阴极) |
| C.NaOH溶液(阴极) | D.Na2SO4(阳极) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-===Fe(OH)2 |
| C.电池充电过程中,阴极附近溶液的pH降低 |
| D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.脱氧过程是吸热反应,可降低温度,延长食品保质期 |
| B.脱氧过程中铁作原电池正极,电极反应为:Fe-3e-=Fe3+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e-=4OH- |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com