
| A. | 它是第Ⅷ族元素 | |
| B. | 它是第六周期元素 | |
| C. | 它属于过渡元素 | |
| D. | 它的某种同位素核内中子数大于质子数 |
科目:高中化学 来源: 题型:选择题
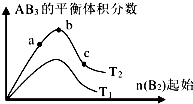
| A. | 反应速率a>b>c | |
| B. | 达到平衡时 A2的转化率大小为:b>a>c | |
| C. | 若T2>T1,则正反应一定是吸热反应 | |
| D. | 达到平衡时,AB3的物质的量大小为:b>c>a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
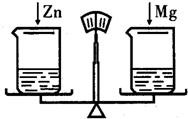 在托盘天平的两托盘上各放一只烧杯,分别注人足量的稀盐酸,天平平衡.向左边烧杯中加入10克金属锌,向右边烧杯中加入10克金属镁,当反应停止后,天平指针的指向是( )
在托盘天平的两托盘上各放一只烧杯,分别注人足量的稀盐酸,天平平衡.向左边烧杯中加入10克金属锌,向右边烧杯中加入10克金属镁,当反应停止后,天平指针的指向是( )| A. | 分度盘的左边 | B. | 分度盘的中间 | ||
| C. | 分度盘的右边 | D. | 三种情况都有可能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在空气中燃烧都能生成过氧化物 | |
| B. | 与盐酸溶液反应时都能生成碱和氢气 | |
| C. | 熔沸点随原子序数增加而升高 | |
| D. | 还原性随原子电子层数的增加而增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3 | B. | CuSO4 | C. | NaOH | D. | NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、SO42-、OH- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、H+、Cl-、HCO32- | D. | Na+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
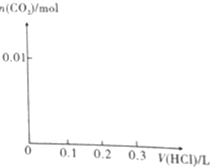 (1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.在如图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.
(1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.在如图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 ;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).
;该物质溶于水后的溶液呈碱性(填“酸”、“碱”或“中”).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com