
| A. | 苯酚遇石蕊显红色 | B. | 包装用材料聚氯乙烯属于烃 | ||
| C. | 食用花生油能发生水解反应 | D. | PX项目中的对二甲苯属于饱和烃 |
科目:高中化学 来源: 题型:选择题
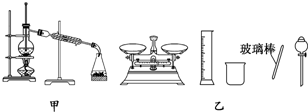
| A. | 用托盘天平称取10.60 g的Na2CO3固体,溶于1 L的水可配成0.1 mol/L的溶液 | |
| B. | 实验室蒸馏石油可用如图甲所示实验装置 | |
| C. | 取用金属钠或钾时,没用完的钠或钾要放回原瓶 | |
| D. | 配制500 mL 0.4 mol/L NaCl溶液,必要的仪器如图乙所示 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
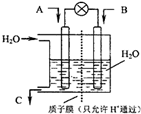 面对全球近期的气候异常,环境问题再次成为焦点.SO2、NOx、CO2是对环境影响较大的气体,对他们的合理控制和治理是优化我们生存环境的有效途径.
面对全球近期的气候异常,环境问题再次成为焦点.SO2、NOx、CO2是对环境影响较大的气体,对他们的合理控制和治理是优化我们生存环境的有效途径.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加热灼烧的方法鉴别铁粉和炭粉 | |
| B. | 用酚酞溶液鉴别未知浓度的NaOH溶液和Na2CO3溶液 | |
| C. | 用丁达尔效应鉴别FeCl2溶液和FeCl3溶液 | |
| D. | 用氨水鉴别MgSO4溶液和Al2(SO4)3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发、结晶 | B. | 过滤、分液 | C. | 过滤、蒸馏 | D. | 萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
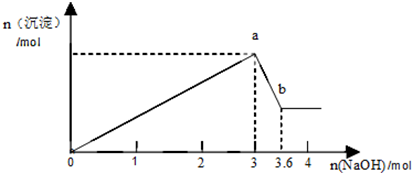
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 用电解水的方法制取大量氢气可以缓解能源不足的问题 | |
| D. | 升高温度活化能降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
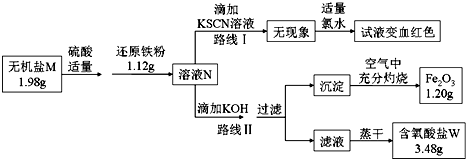
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com