
| A. | 单质的沸点:Z>X>W | |
| B. | 原子半径:Z>Y>X>W | |
| C. | WX与ZX中的化学键类型相同 | |
| D. | 当W的化合价为+4时,W与X只能形成一种化合物 |
分析 短周期元素W、X、Y、Z 的原子序数依次增大,W的单质是空气中体积分数最大的气体,W为N;Z原子的最外层电子数等于最内层电子数,Z应为第三周期元素,最外层电子数为2,则Z为Mg;X、Y、Z简单离子的电子层结构相同,均为10电子的离子,W与Y原子的最外层电子数之和等于X原子的最外层电子数,Y应为第三周期元素Na,则X的最外层电子数为5+1=6,且X的原子序数小于Y、Z 的原子序数,X为O,以此来解答.
解答 解:由上述分析可知,W为N,X为O,Y为Na,Z为Mg,
A.常温下Mg为固体,氮气与氧气为气体,且氧气的相对分子质量较大,则单质的沸点:Z>X>W,故A正确;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径:Y>Z>W>X,故B错误;
C.NO只含共价键,MgO中的化学键为离子键,故C错误;
D.当W的化合价为+4时,W与X能形成NO2、N2O4,故D错误;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、原子序数来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | SiO2与水反应生成酸 | B. | O元素原子的第二层电子数为8 | ||
| C. | SiO2可与氢氧化钠反应 | D. | SiO2与干冰、冰属于同一类晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
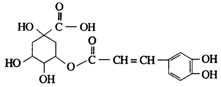 金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )| A. | 绿原酸的分子式为C16H8O9 | |
| B. | 1个绿原酸分子中含有4个手性碳原子 | |
| C. | 1mol绿原酸最多与4molNaOH反应 | |
| D. | 1mol绿原酸最多能与6molH2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①中Se是还原产物,I2是氧化产物 | |
| B. | 反应②中浓H2SO4是氧化剂,SeO2是氧化产物 | |
| C. | 反应①中每生成1.0 mol I2,转移2.0 mol电子 | |
| D. | Se、KI、SO2的氧化性由强到弱的顺序是K I>Se>SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 和
和 ⑤
⑤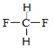 和
和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com