
某化学研究性学习小组为了解Cu的常见化合物性质,运用类比的思想提出如下问题,并进行探究。
提出问题 ①通常情况下,+2价Fe不如+3价Fe稳定,+1价Cu也不如+2价Cu稳定吗?
②CuO能被H2、CO等还原,也能被NH3还原吗?
实验方案 (1)解决问题①的实验步骤和现象如下:取98 g Cu(OH)2固体,加热至80 ℃~100 ℃时,得到黑色固体粉末,继续加热到1 000 ℃以上,黑色粉末全部变成红色粉末A。冷却后称量,A的质量为72 g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器内还有红色固体存在。据此可推得A的化学式为____________。
(2)如图所示为常见气体的制备、干燥和性质验证的部分仪器装置(部分夹持装置及尾气处理装置未画出),请从中选择合适的药品和仪器装置回答问题。
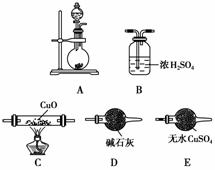
①制取干燥的NH3并还原CuO,所选仪器装置的正确连接顺序是________。
②制取NH3可选用下列药品中的________。
A.NH4Cl和Ca(OH)2 B.NH4HCO3
C.浓氨水和生石灰 D.浓氨水和固体烧碱
③若CuO能被NH3还原,实验中观察到的现象是________________________,该反应的化学方程式为__________________________。
实验结论 根据“实验方案(1)”,得出的+1价Cu和+2价Cu稳定性大小的结论是________________________________________________________________________。
科目:高中化学 来源: 题型:
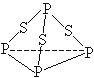
三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热△H=-3677kJ/mol(P被氧化为P4O10),下列有关P4S3的说法中不正确的是( )
A.分子中每个原子最外层均达到8电子稳定结构
B.P4S3中硫元素为-2价磷元素为+3价
C.一个P4S3分子中含有三个非极性共价键
D.热化学方程式为P4S3( s)+8O2(g) =P4O10(s )+3SO2(g) △H=-3677kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中:①乙烷;②苯;③聚丙烯;④聚异戊二烯;⑤2-丁炔;⑥环己烷;⑦邻二甲苯;⑧裂解气,能使酸性KMnO4溶液褪色,也能与溴水反应而使溴水褪色的是( )
A.②③④⑤⑥⑦⑧ B.③④⑤⑥⑦⑧ C.④⑤⑧ D.④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下图中各物质的转化关系。
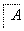
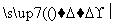
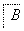
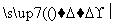
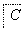
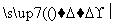
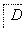
已知A是地壳中含量最高的金属元素单质。
(1)写出B、D的化学式:B________;D________。
(2)写出离子方程式:
C→D_______________________________________________________;
B+CO2→D__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.铁是人类在生产、生活中最早使用的金属
B.金、银、铜是应用最广泛的金属材料
C.钛被誉为“21世纪的金属”,应用前景很广阔
D.铜是导电性、导热性最好的有色金属
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化。
(1)该同学最初的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅰ | 先向2 mL 0.1 mol·L-1 FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | |
| Ⅱ | 先向2 mL 0.1 mol·L-1 FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol·L-1 KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加KI溶液后,血红色无明显变化 |
①实验Ⅰ的现象为___________________________________________________。
②FeCl2溶液与新制氯水反应的离子方程式为_____________________________
______________________________________________________________________。
(2)该同学分析了导致实验Ⅱ现象的可能原因,并对实验方案进行了改进。改进后的实验操作和现象如下:
| 编号 | 操作 | 现象 |
| Ⅲ | 向2 mL 0.1 mol·L-1 KI溶液中滴加1 mL 0.1 mol·L-1 FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
根据实验Ⅲ,该同学认为Fe3+有可能与I-发生氧化还原反应,请结合实验现象用简明的文字说明他得出上述结论的理由:_____________________________________。
(3)该同学认为需要进一步设计实验,证明根据实验Ⅲ中现象得出的结论。请补全下表中的实验方案:
| 编号 | 操作 | 预期现象及结论 |
| Ⅳ | 向2 mL 0.1 mol·L-1 KI溶液中滴加1 mL 0.1 mol·L-1 FeCl3溶液,__________ |
(4)上述实验结果表明,Fe3+有可能与I-发生氧化 还原反应。进一步查阅资料知,参加反应的Fe3+与I-的物质的量相同。该同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变红的原因,认为Fe3+与I-反应的离子方程式应写为__________________________________________。
还原反应。进一步查阅资料知,参加反应的Fe3+与I-的物质的量相同。该同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变红的原因,认为Fe3+与I-反应的离子方程式应写为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为了探究AgNO3的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用第试剂KSCN溶液、K3[Fe(CN)6]溶液、氯水。
(1)请完成下表:
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | ① | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入 ② ,振荡 | ③ | 存在Fe2+ |
【实验结论】Fe的氧化产物为存在Fe2+和Fe3+
Ⅱ. AgNO3的热稳定性性
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束以后,试管中残留固体为黑色。
(2)装置B的作用是 。
(3)经小组讨论并验证该无色气体为O2,其验证方法是 。
(4)【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水。
【提出假设】试管中残留的黑色固体可能是:ⅰAg;ⅱ.Ag2O;ⅲ.Ag和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验。
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硫酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验评价】根据上述实验,不能确定固体产物成分的实验是 ① (填实验编号) 。
。
【实验结论】根据上述实验结果,该小组得出的AgNO3固体热分解的产物有 ② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
依据元素周期表及元素周期律,下列推断正确的是( )
A. H3BO3的酸性比H2CO3的强
B. Mg(OH)2的碱性比Be(OH)2的强
C. HCl、HBr、HI的热稳定性依次增强
D. 若M+和R2﹣的核外电子层结构相同,则原子序数:R>M
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4 + 5H 2C2O4 + 3H2SO4 === K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
【实验内容及记录】
| 实验编号 | 温度/℃ | 试管中所加试剂及其用量/ mL | 溶液褪至无色所需时间/ min | |||
| 0.6 mol/L | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L | |||
| 1 | 20 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 20 | 3.0 | m | 2.5 | n | 4.8 |
| 3 | 20 | 3.0 | 3.0 | 2.0 | 2.0 | t1 |
| 4 | 30 | 3.0 | 2.0 | 3.0 | 2.0 | t2 |
(1)已知:实验1、2、3的目的是探究KMnO4浓度对反应速率的影响。则实验2中m= ,
n= 。如果研究温度对化学反应速率的影响,需利用实验4和 。
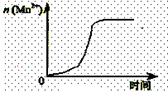 (2)通过查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势如右图所示。为进行实验探究,该小组同学通过讨论提出假设:Mn2+对该反应有催化作用。
(2)通过查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势如右图所示。为进行实验探究,该小组同学通过讨论提出假设:Mn2+对该反应有催化作用。
①请你填写表中空白帮助该小组同学完成实验方案。
| 实验编号 | 温度/℃ | 试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 溶液褪至无色所需时间/ min | |||
| 0.6 mol/L | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L | ||||
| 5 | 20 | 3.0 | 2.0 | 3.0 | 2.0 |
| t3 |
②能说明该小组同学提出的假设成立的实验事实是 。
(3)有人将酸性KMnO4 溶液和H 2C2O4 溶液的反应设计成原电池,则该原电池的正极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com