
| A. | 再滴加AgNO3溶液,观察是否有AgI沉淀产生 | |
| B. | 加入CCl4振荡后,观察下层液体颜色 | |
| C. | 加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察是否出现红色 | |
| D. | 加入CCl4振荡后,取上层清液,滴加入AgNO3溶液,观察是否有AgCl沉淀产生 |
分析 三氯化铁中加过量的碘化钾,充分反应后加硫氰化钾,溶液变血红色,证明有三价铁离子存在,从而证明FeC13溶液和KI溶液的反应存在反应限度,以此解答该题.
解答 解:A.加入FeCl3溶液5~6滴,物质的量较少,由于有KI的剩余,滴加AgNO3溶液,肯定会有黄色沉淀生成,不能判断2Fe3++2I-?I2+2Fe2+是否存在限度,故A错误;
B.由于加入FeCl3溶液,将碘离子氧化为碘单质,加入CCl4振荡后,生成的碘单质溶于CCl4而显紫红色,智能说明生成了碘单质,而不能判断是否存在限度,故B错误;
C.滴加KSCN溶液,观察溶液是否变血红色,说明溶液中存在铁离子,由于加入FeCl3溶液较少,若不存在限度,加入KSCN溶液后,溶液是不变色,说明该反应存在限度,故C正确;
D.加入AgNO3溶液,有白色沉淀生成,说明存在,由于氯离子不参与离子反应,即氯离子始终存在于溶液中,所以不能判断是否存在限度,故D错误.
故选C.
点评 本题考查可逆反应特点及应用,为高频考点,题目难度不大,明确铁离子的检验方法为解答关键,注意掌握可逆反应特点,试题培养了学生的分析能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 相同物质的量浓度的下列溶液:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3•H2O; c(NH4+)由大到小的顺序是:①>②>③>④ | |
| B. | 某溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,则该溶液的pH一定为14-a | |
| C. | 物质的量浓度相等的 H2S 和 NaHS 混合溶液中:c(Na+)=2c(S2-)+2c(HS-)+2c(H2S) | |
| D. | 常温下,若0.1mol/L NaHY溶液的pH=4,该溶液中粒子浓度关系为:c(Na+)>c(HY-)>c(Y2-)>c(H+)>c (H2Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 126C和146C互为同位素 | |
| B. | 金刚石和石墨互为同素异形体 | |
| C. | CH3COOCH2CH3和CH3CH2CH2COOH互为同分异构体 | |
| D. | CH4和CH3Cl互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯锌与稀硫酸反应比粗锌的反应速率快 | |
| B. | 用稀硫酸与锌制取氢气时,加入少量硫酸铜溶液,可加快反应的速率 | |
| C. | 纯铁比生铁更难发生电化学腐蚀 | |
| D. | 钢铁腐蚀主要是吸氧腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱、纯碱、熟石灰均属于碱 | |
| B. | 稀豆浆、FeCl3溶液、牛奶均属于胶体 | |
| C. | HCl、BaSO4、NH3•H2O均属于电解质 | |
| D. | MgO、CuO、Na2O2均属于碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
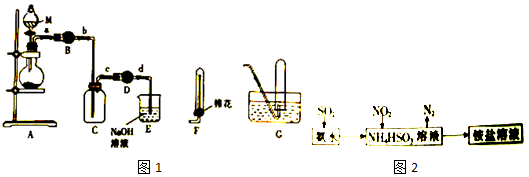
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原CuSO4溶液的浓度为0.1mol/L | |
| B. | 反应过程中共转移0.02mol电子 | |
| C. | 向电解后的溶液中加入适量CuO,可恢复到原溶液 | |
| D. | 阳极周围溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com