
| A、钠 | B、铜 | C、铝 | D、铁 |
| 0.3mol |
| 0.1mol |
| 0.2mol |
| 0.1mol |


科目:高中化学 来源: 题型:
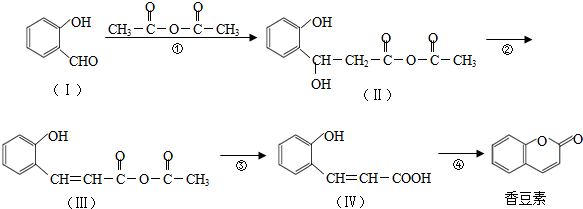
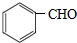 与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为
与CH3CHO能发生类似反应①、②的两步反应,最终生成的有机物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应处于平衡状态时,c(NH3)?c(O2)=c(NO)?c(H2O) |
| B、反应达到平衡后,ν正(NH3)=ν逆(H2O) |
| C、其它条件不变,温度越高,氨的转化率越高 |
| D、寻找合适的催化剂是加快反应速率并提高NO产率的有效措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 适量稀硝酸 |
| 过量铁粉 |
| 足量稀硫酸 |
| 过滤、洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.44g | B、1.6g |
| C、2.82g | D、4.36g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
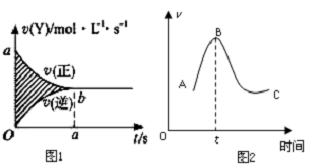 (1)在容积固定的4L密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图1.则图中阴影部分的面积表示
(1)在容积固定的4L密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t的关系如图1.则图中阴影部分的面积表示查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③④⑦⑧ | B、①⑥⑦⑧⑨ |
| C、②④⑧⑨⑩ | D、②④⑥⑦⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com